二次進行形多発性硬化症の新たな病態メカニズムを発見
九州大学は1月28日、二次進行形多発性硬化症の新たな病態メカニズムを発見したと発表しました。脳・脊髄のグリア細胞同士をつなぐ「ギャップ結合蛋白」がグリア炎症を制御しており、これらの機能異常が多発性硬化症の進行に大きく関わっているそうです。
この研究成果は、同大大学院医学研究院の吉良潤一教授、山﨑亮准教授、山口浩雄共同研究員、大学院医学府博士課程4年の趙奕楠、博士課程1年の永田諭らの研究グループによるもの。1月13日付で米国科学アカデミー紀要(PNAS)に掲載されています。
多発性硬化症は、発症初期は症状が自然に良くなりますが、発症10年後ごろから症状が治らなくなり、やがて再発していないにもかかわらず、症状が次第に進行する「二次進行型」に移行します。現在、再発寛解型の再発を減らす薬は保険診療で使用できますが、二次進行形に移行すると、そのメカニズムが不明で有効な治療薬は開発されていませんでした。
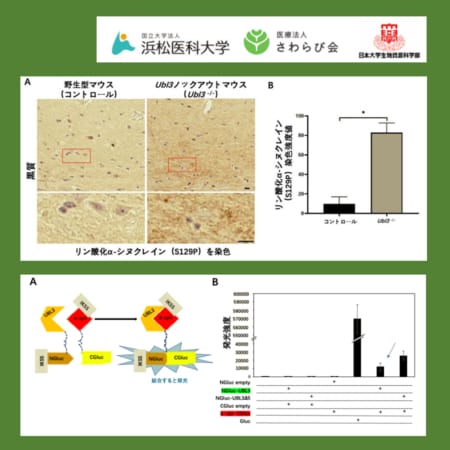
今回、研究グループは、多発硬化症モデルマウスで中枢神経の髄鞘を産生するオリゴデンドログリアのギャップ結合蛋白「コネキシン47」を特異的に喪失させると、中枢神経のグリア細胞が異常に活性化し、末梢血から自己免疫細胞を呼び込み、髄鞘が破壊されることにより、二次進行型と同様の症状と経過を示すことを世界で初めて発見しました。
マウスでみられたグリア細胞の活性化やコネキシン蛋白の発現変動は、これまでも多発性硬化症患者さんの脳・脊髄の解剖で見られていたそうですが、その原因や意義はこれまで不明でした。
今回の成果について、研究グループは以下の通りコメントしています。
この研究により、コネキシン蛋白の機能を修飾することで、これまでになかった二次進行形多発性硬化症の新規治療薬が開発できる可能性が高くなりました。既に同研究グループではコネキシン機能を修飾するいくつかの薬剤の効果がこのマウスモデルを使ってみられています。
http://www.kyushu-u.ac.jp/ja/researches/view/418
多発性硬化症とは
国指定の難病である多発性硬化症は、原因が解明されておらず、根治療法はありません。自己免疫機序によって脳や脊髄、視神経など中枢神経の神経突起を取り巻く「髄鞘」が繰り返し障害され、感覚低下や運動麻痺、視力障害、言語障害、歩行障害、排尿・排便障害などさまざまな神経症状が起こります。
近年、増加が著しく、我が国で約2万5千人、世界では250万人以上の患者さんがいます。この病気は1:3の割合で女性に多く、20歳代から30歳代の若年成人が侵されやすく、発病すると終生罹患するため、大きな社会問題となっています。
出典元
九州大学 研究成果
※再発性多発性硬化症の患者さん対象、医師主導治験のお知らせ