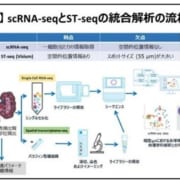
デュシェンヌ型筋ジストロフィーに対するEMBARK試験のトップライン結果を発表
中外製薬株式会社は、戦略的アライアンスを締結しているスイス・ロシュ社が10月30日、歩行可能なデュシェンヌ型筋ジストロフィーの4歳~7歳の男児を対象としたElevidys(delandistrogene moxeparvovec:SRP-9001)のグローバル第III相ランダム化二重盲検多施設共同EMBARK試験のトップライン結果を発表したと報告しました。
デュシェンヌ型筋ジストロフィーは、ジストロフィン遺伝子変異により発症し、小児の早期から急速に進行する希少な遺伝性の消耗性筋疾患です。ジストロフィンというタンパク質が作られないため、筋組織の瘢痕化や脂肪化が徐々に進行します。
Elevidysは、デュシェンヌ型筋ジストロフィーに対して初めて承認された遺伝子治療薬であり、標的とする骨格筋や呼吸筋、心筋において、短縮型ジストロフィンの発現を介し、デュシェンヌ型筋ジストロフィーの原因に働きかけるようデザインされています。
EMBARK試験は、歩行可能なデュシェンヌ型筋ジストロフィーの4歳~7歳の男児を対象にElevidysを単回投与する群とプラセボを投与する群に振り分け、Elevidysの有効性と安全性を評価した第III相試験です。
その結果、ノース・スター歩行能力評価(North Star Ambulatory Assessment:NSAA)による総スコアは、52週時点では、Elevidys群2.6ポイントの向上であったのに対し、プラセボ群は1.9ポイントの向上であり、主要評価項目の達成には至りませんでしたが数値上の向上は認められました。
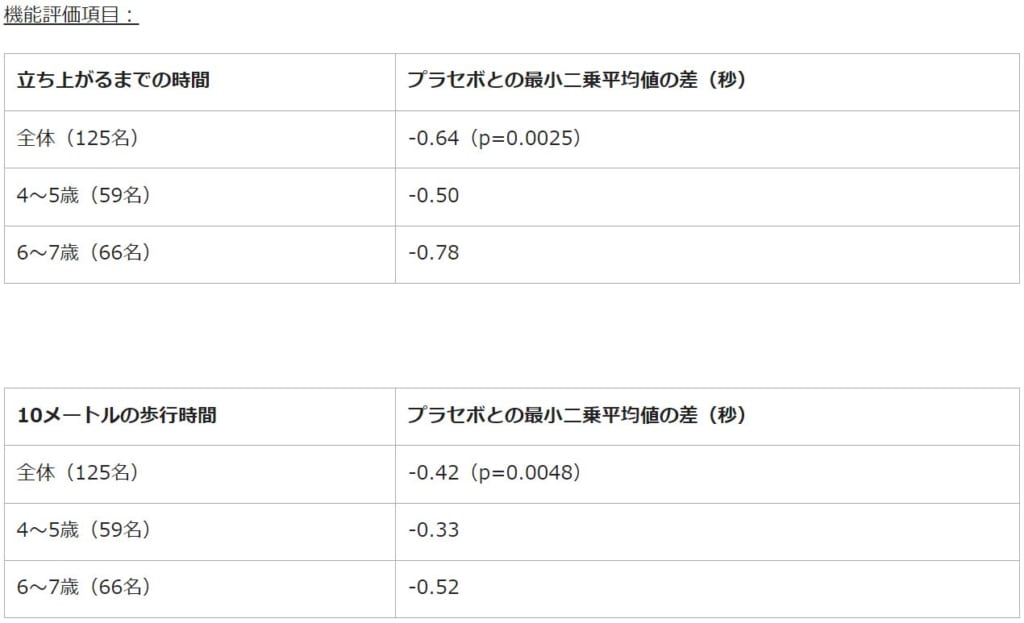
一方、事前に規定された時間機能に関する重要な副次的評価項目である、床から立ち上がるまでの時間と10メートルの歩行時間は、どちらもElevidys投与群において統計学的に有意な改善が認められました。また、日中の最高歩行速度を測定するウェアラブルデバイス(Syde)を用いたStride Velocity 95th Centile(SV95C)においても、臨床的に意義があり、統計学的有意な改善が認められました。
なお、試験の詳細は解析中であり、今後の開発計画について検討するために規制当局と協議予定であり、試験の詳細な結果は、今後の医学系学会で発表され、医学論文に掲載される予定です。