皮膚エリテマトーデス(CLE)に対するlitifilimab、第II相試験で良好な結果を報告
米バイオジェン社は3月28日、皮膚エリテマトーデス(CLE)患者を対象とするlitifilimabの第II/III相試験(AMETHYST試験)の第II相パート(パートA)のポジティブな結果を発表しました。
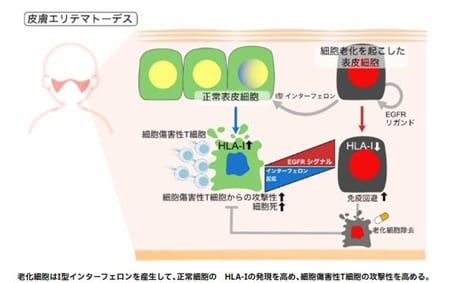
皮膚エリテマトーデス(CLE)は、皮膚に発疹、痛み、かゆみなどの症状が現れ、進行すると回復の困難な傷跡や脱毛などを引き起こす自己免疫疾患です。現在、同疾患を標的とした承認済みの治療薬はありません。
AMETHYST試験は、進行中の連続した2つのパートからなる多施設共同二重盲検プラセボ対照無作為化試験で、様々な重症度の皮膚エリテマトーデス(CLE)患者さんを対象にlitifilimabの有効性と安全性をプラセボと比較して評価します。litifilimabは、16週間投与された時点での患者さんの皮膚の症状を、プラセボを投与されたグループと比較して疾患活動性の有意な低下を示し、主要な目標を達成しました。また、安全性についても、これまでの試験と同様に概ね高い忍容性が確認され、副作用の多くは軽度または中等度でした。
litifilimabは、特定の免疫細胞の働きを抑えることで炎症を鎮める新しいタイプの薬剤です。今回の結果は、米国食品医薬品局による画期的治療薬の指定を支持するものであり、承認されれば、皮膚エリテマトーデス(CLE)に対する約70年ぶりの革新的な新薬となる可能性があります。現在、試験は最終段階である第Ⅲ相部分へと進んでいます。
UTサウスウェスタン・メディカル・センターの皮膚科学教授兼講座主任およびリウマチ疾患部門内科学教授のジョセフ・F.メローラ医師はプレスリリースにて、「私たちは今回litifilimabの2つの第II相試験から、CLEにおける皮膚の疾患活動性の目覚ましい低下を示す一貫した結果を得ました。これは本開発プログラムにおける重要な節目と言えます。今回の結果は、現在承認され標的治療薬がなく、重大なアンメットニーズが存在する皮膚エリテマトーデスの患者さんにlitifilimabを提供できる可能性を裏付けるものであり、私はこの結果を心強く感じています。これらの知見は、FDAによるブレイクスルーセラピーの指定とともに、承認されれば、この困難な疾患を抱える患者さんにもたらし得るlitifilimabの可能性を示しています。」と述べています。
また、バイオジェンのチーフ・メディカル・オフィサーであるダニエル・カーク氏は、「皮膚エリテマトーデスは肌に瘢痕を残すだけでなく、この疾患を抱える人々に大きな精神的かつ社会的な影響をおよぼす可能性があります。承認された疾患標的修飾薬は存在せず、CLE患者さんの選択肢は非常に限られています。この疾患の代表的な集団においてLitifilimabが総じて高い忍容性を示し、皮膚疾患の改善と関連づけられたことを非常に嬉しく思います。第III相プログラムを進める上で大きな追い風となります。バイオジェンがループスで、特にCLEで達成した成果は、選択肢が限られている、または存在しない疾患に取り組む当社のコミットメントを表しています」と述べています。