前頭側頭葉変性症(FTLD)の治療薬候補を発見、標的分子をiPS創薬で同定
京都大学iPS細胞研究所(CiRA)は4月4日、前頭側頭葉変性症(FTLD)の患者さんのiPS細胞を用いた既存薬スクリーニングにより、治療薬候補を発見し、その作用標的となる分子を同定したと発表しました。
前頭側頭葉変性症(指定難病127、FTLD)は、若年性認知症の主な原因の一つであり、性格変化や言語障害、運動機能の低下などを引き起こす疾患です。根本的な治療法は確立されておらず、新たな治療法の開発が強く望まれています。前頭側頭葉変性症(FTLD)の原因の一つとして、脳内にタウやTDP-43といった異常なタンパク質が蓄積することが知られており、特にタウオリゴマーと呼ばれる異常な形をしたタウタンパク質が蓄積することが、神経細胞に有害であると考えられています。
研究グループはこれまで、前頭側頭葉変性症(FTLD)の一種であるFTLD-Tauの患者さんのiPS細胞を用いた研究で、神経細胞におけるタウオリゴマーの蓄積や神経細胞の過剰な興奮などを明らかにしてきました。
今回の研究では、FTLD-Tau患者さんのiPS細胞から作製した神経細胞を用いて、治療薬の候補となる既存薬のスクリーニングを実施。その結果、他の脳疾患の治療に用いられているガバペンチンという既存薬が、タウオリゴマーの蓄積を抑制し、神経細胞死を防ぐ効果を示すことがわかりました。さらに、プレガバリンやミロガバリンといったガバペンチノイドと呼ばれる類似の薬も、同様の効果を発揮しました。これらの薬剤は、電位依存性カルシウムチャネルのα2δサブユニットに結合することが知られており、その中でもα2δ1とα2δ2の2つのタイプが標的となります。
そこで、研究グループは、どちらのサブユニットがFTLD-Tauの病態に関与しているかを特定するため、患者さんのiPS細胞を用いて、CACNA2D1(α2δ1をコードする遺伝子)とCACNA2D2(α2δ2をコードする遺伝子)のノックアウト実験を行いました。その結果、CACNA2D2をノックアウトすることで、FTLD-Tauの神経細胞死とタウオリゴマーの蓄積が抑制され、α2δ2がFTLD-Tauの神経変性において重要な役割を果たしていることが明らかになりました。さらに、患者さんのiPS細胞から作製した脳オルガノイドにおいても同様の神経変性の特徴が確認され、CACNA2D2遺伝子をノックアウトすることで、関連する遺伝子発現の異常が一部改善しました。これらの結果は、α2δ2がFTLD-Tauの新たな治療標的となる可能性を示唆しています。
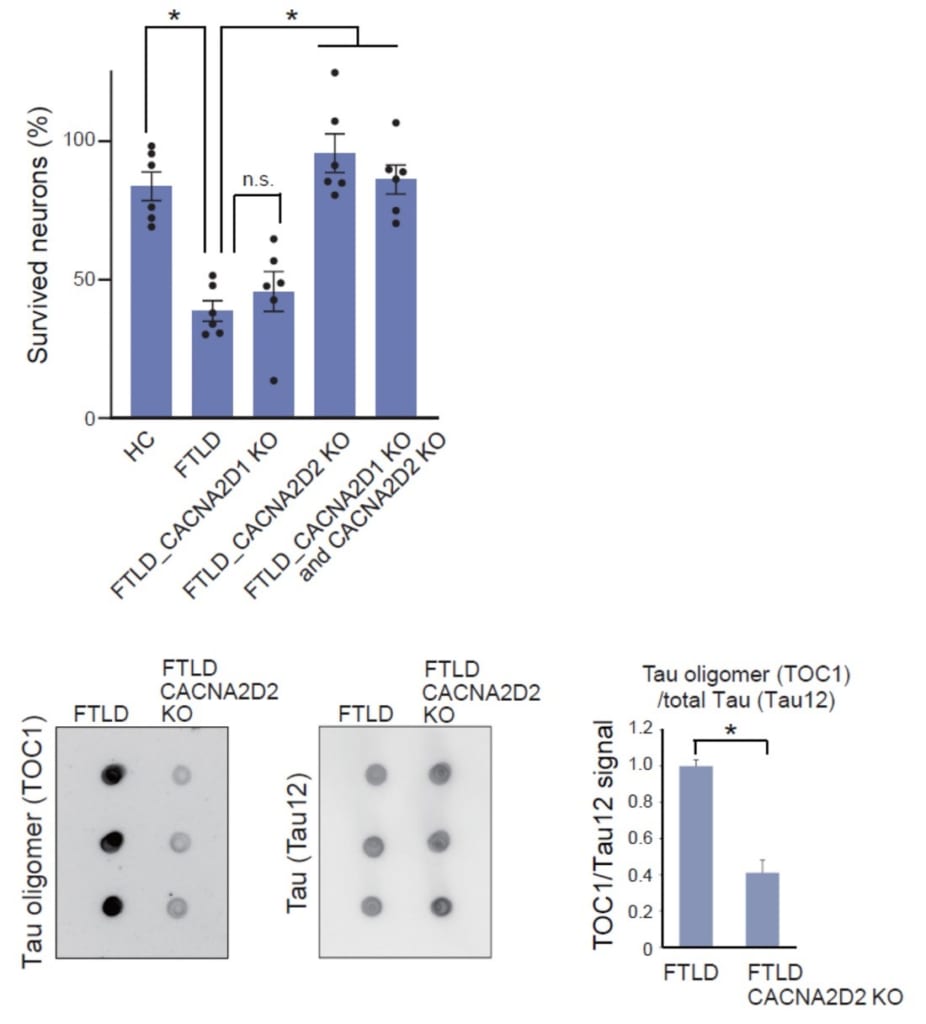
以上の研究成果より、FTLD-Tau患者さんのiPS細胞を用いた薬剤スクリーニングと詳細なメカニズム解析を通じて、CACNA2D2遺伝子がコードするα2δ2がFTLD-Tauの治療標的となりうる可能性が示されました。また、CACNA2D2を標的とする既存薬であるガバペンチン、プレガバリン、ミロガバリンが、前頭側頭葉変性症(FTLD)の治療薬として応用できる可能性が示唆されました。
なお、同研究の成果は、「European Journal of Cell Biology」オンライン版に3月29日付で掲載されました。