重症血友病Aの乳児に対するヘムライブラ、第III相試験において早期予防投与のベネフィットを確認
中外製薬株式会社は12月11日、未治療または治療歴の短い血液凝固第VIII因子に対するインヒビター非保有の重症血友病Aの乳児を対象とした第III相HAVEN7試験の主要解析において、へムライブラ(一般名:エミシズマブ、以下ヘムライブラ)の有効性および安全性が裏付けられたと発表しました。
血友病Aは、血を固める働きをする血液凝固因子が生まれつき不足または欠損している病気です。幼少期から出血しやすく、頭蓋内、関節内、筋肉内など、体の深部で出血が多く発生します。現在、低年齢で定期的な出血抑制を目的とする治療を開始することが血友病の標準治療とされていますが、多くの血友病Aの乳児では、生後1年までは出血抑制を目的とする治療が開始されていません。
へムライブラは、中外製薬独自の抗体エンジニアリング技術を用いて創製されたバイスペシフィック抗体です。同剤は活性型第IX因子と第X因子に結合し、活性型第IX因子による第X因子の活性化反応を促進することで、血友病Aで欠損または機能異常を来している第VIII因子の補因子機能を代替します。ヘムライブラは、既に乳児に対しても承認を取得しており、出生時から皮下投与が可能です。また、維持投与においては複数の投与間隔レジメンにより柔軟な治療選択が可能であるという特徴があります。
HAVEN7試験は、血液凝固第VIII因子に対するインヒビターを保有しない重症血友病Aの乳児55名を対象としたへムライブラの有効性、安全性、薬物動態および薬力学を評価した記述的な第III相単群試験です。同試験は、血友病Aコミュニティと協働して実施されました。
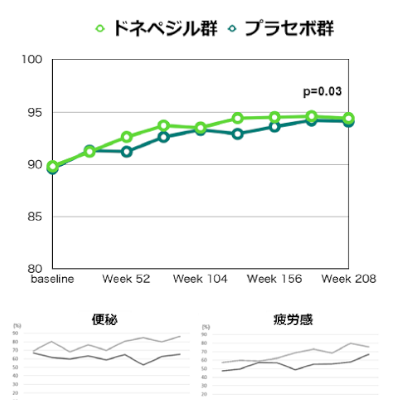
その結果、追跡調査機関中央値101.9週間時点で、治療を要する出血が認められなかった被験者の割合は54.5%(30名)、治療の要否にかかわらずすべての出血が認められなかった被験者の割合は16.4%(9名)でした。治療を要する自然出血が認められた被験者は0名で、治療を要した出血はすべて外傷性でした。血液凝固第VIII因子インヒビター陽性となった被験者は3.6%(2名)であり、これはヘムライブラの投与により第VIII因子製剤の使用が少なかったことが理由と推察されました。また、抗薬物抗体陽性となった被験者はいませんでした。
今回の試験結果は、中間解析およびこれまでに実施された第III相HAVEN試験群の肯定的な結果と同様であり、新たな安全性シグナルは認められず、本剤と関連のある重篤な有害事象、頭蓋内出血または死亡は報告されませんでした。
さらに、バイオマーカーの追加研究が実施され、その結果は、本試験の有効性に関する主要解析を支持するものでした。この追加研究により、乳児におけるヘムライブラの薬力学プロファイルは、これまでに、年長の小児および成人の血友病Aで観察されたものと同様であることが示されました。ヘムライブラが結合する凝固因子の存在量が少ない年齢層であり、ヘムライブラが想定される薬力学的反応を示すことが明らかになりました。
中外製薬代表取締役社長CEOの奥田修氏は「重症血友病Aに対する出血抑制を目的とした治療において、静脈内投与が困難な乳児に対し、皮下投与可能なヘムライブラは治療負担を軽減する選択肢となります。今回の試験では、乳児に対して初めて、ヘムライブラが有効な出血コントロールを示しました。これは、これまでに実施された臨床試験において示された幅広い年齢層におけるデータを補完し、ヘムライブラによる乳児における出血抑制を目的とした治療をより早期に開始することを支持するものです。本剤を必要とする方々により安心してお使いいただけるよう、長期データの収集をはじめ、引き続きエビデンスの構築に努めてまいります」と述べています。
なお、同研究および追加研究の成果は、12月9~12日にカリフォルニア州サンディエゴで開催された第65回米国血液学会(ASH)年次総会で発表され、プレスプログラムにも採択されました。