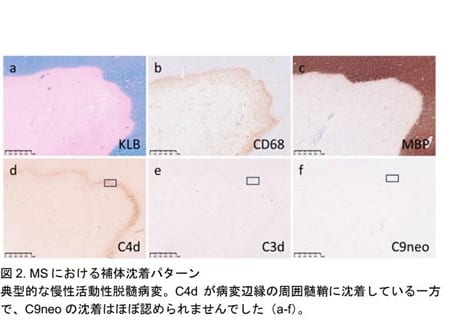
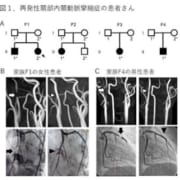
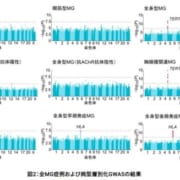
ウルリッヒ型先天性筋ジストロフィー(UCMD)モデルマウスへの間葉系間質細胞移植、XF-iMSCがもっとも安全かつ効果的な候補に
京都大学iPS細胞研究所(CiRA)の研究グループは10月7日、ウルリッヒ型先天性筋ジストロフィー(UCMD)モデルマウスに対して、脂肪・骨髄・iPS細胞由来の間葉系間質細胞(MSCs)の細胞治療効果を比較し、iPS細胞由来の間葉系間質細胞(XF-iMSCs)がもっとも安全かつ効果的な候補となりうることを明らかにしたと発表しました。
ウルリッヒ型先天性筋ジストロフィー(UCMD)は、幼少期に発症する進行性の疾患で、遺伝子変異により6型コラーゲン(COL6)が欠乏し、細胞外マトリックスの構造と特性が変化し、ミトコンドリアの欠陥や筋再生の障害を引き起こします。その症状は、筋肉の弱さ、関節の過伸展性、および進行性の関節拘縮を特徴としています。現在、ウルリッヒ型先天性筋ジストロフィー(UCMD)の有効な治療法は確立されていません。
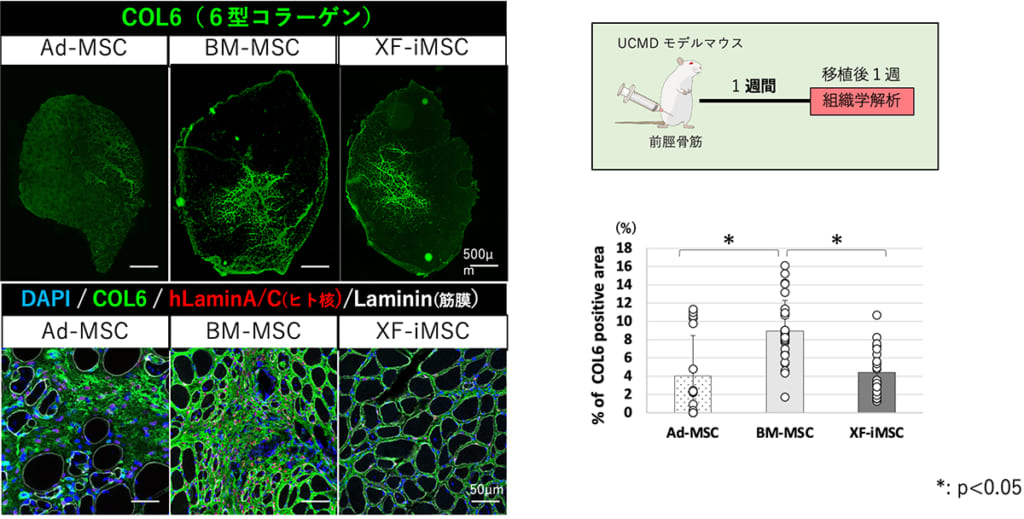
今回、研究グループは、ウルリッヒ型先天性筋ジストロフィー(UCMD)モデルマウスの前脛骨筋に、3種類のMSC(Ad-MSCs、BM-MSCs、XF-iMSCs)をそれぞれ移植しました。移植の1週間後、すべてのMSCで生着が認められ、COL6が補充されました。筋肉の総面積に対するCOL6陽性領域の割合は、BM-MSCを移植した群で、他の2種類の細胞を移植した群よりも有意に高くなりました。
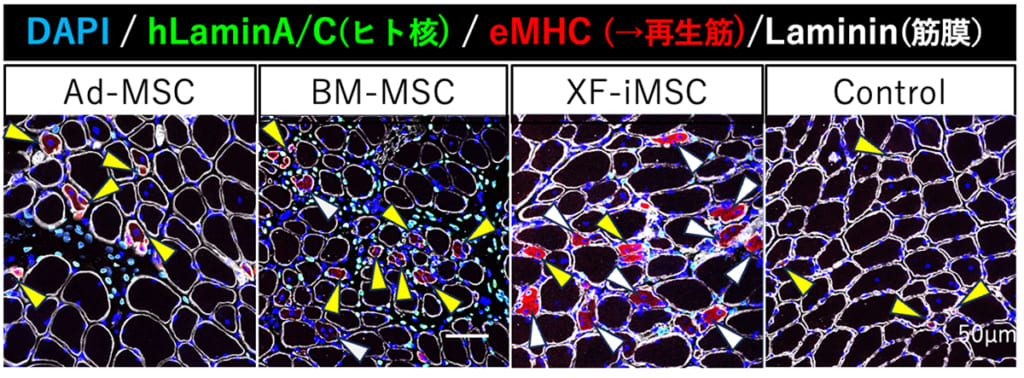
移植から1週間後の筋線維の再生を比較した結果、骨格筋再生時に一過性に発現するeMHCは、コントロール群では非常に小径の線維に限られており、筋の成熟が不完全であることが示されました。XF-iMSCを移植した群では、過去の報告と同様に、多核再生筋線維数の増加と筋線維径の増大が認められました。一方、Ad-MSCs移植群およびBM-MSCs移植群では、白矢頭で示した多核筋線維は観察されたものの、多くの再生筋線維は単核のままでした。
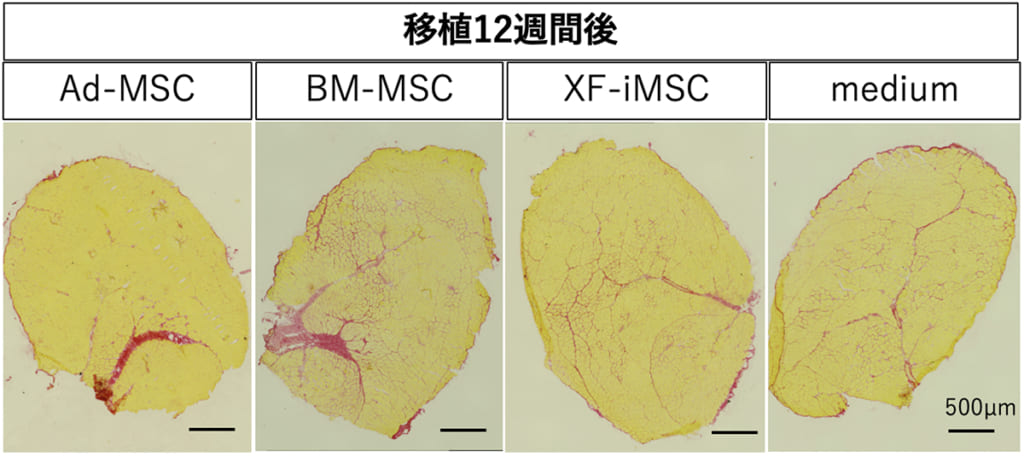
移植から12週間後、移植した細胞が筋肉の病的な線維化に悪影響を及ぼしたかどうかを確認するためにシリウスレッド染色という方法で確認。その結果、BM-MSCs移植群では、間質の拡大を伴う顕著な異所性線維化が認められました。
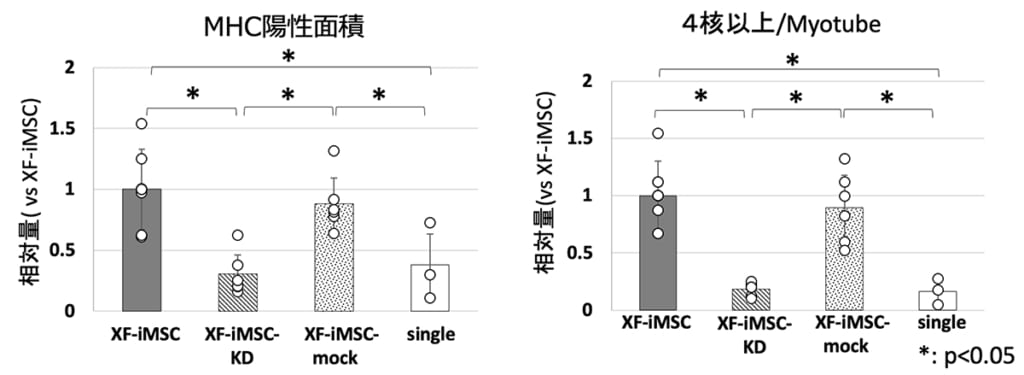
さらに、共培養実験では、XF-iMSCsが他のMSCsよりも効果的にUCMDモデルマウス由来の骨格筋幹細胞の融合と分化を促進することがわかりました。さらに、IGF2の発現をノックダウンしたXF-iMSCs(XF-iMSC-KD)を作成し、無処理のXF-iMSCと比較した結果、F-iMSCsが分泌するIGF2が骨格筋幹細胞の分化を促進することを示唆しました。
以上の研究成果より、XF-iMSCsは筋再生を促進し、線維化を回避する有望な細胞治療の候補であり、他の治療法に比べても安全で効果的なアプローチであると考えられます。
なお、同研究の成果は、「Stem Cell Research&Therapy」に10月7日付で公開されました。