後天性血友病Aにおける出血抑制を効能・効果としてオビザーが製造販売承認を取得
武田薬品工業株式会社は3月26日、遺伝子組換えブタ血液凝固第VIII因子「オビザー静注用500」(一般名:スソクトコグ アルファ(遺伝子組換え)、以下オビザー)について、「後天性血友病A患者における出血抑制」を効能又は効果として、厚生労働省から製造販売承認を取得したと発表しました。
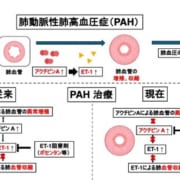
後天性血友病Aは、何らかの機序によって、患者さんが保有する正常な第VIII因子遺伝子に対して、凝結促進作用の機能的欠損を引き起こす自己抗体が出現し、突発的な皮下出血や筋肉内出血などをきたすまれな出血性疾患です。時に重篤な出血症状を呈することがあります。
オビザーは、グリコシル化されたBドメイン欠損遺伝子組換えブタ血液凝固第VIII因子で、後天性血友病Aの成人患者さんにおける出血エピソードのオンデマンド治療薬およびコントロール薬です。
今回の製造販売承認は、主にAHAの日本人18歳以上の患者さん5例を対象とした国内臨床第2/3相試験(NCT04580407)およびAHAの非日本人18歳以上の患者さんを対象とした海外臨床第2/3相試験(NCT01968655)に基づくものです。
国内臨床第2/3相試験において、治療開始から24時間後の時点における、出血コントロール、臨床評価および血液凝固第Ⅷ因子活性に基づく医師評価では、5例全例がオビザーに対して「反応あり」とされました。有害事象は5例に計49件報告され、2例以上に報告された有害事象は皮下出血(3例)および尿路感染(2例)でした。
武田薬品工業株式会社R&D Japanリージョンヘッドの梶井靖氏は「AHAは重篤な出血症状を呈し、生命予後は良好とは言えない難治性の出血性疾患です。オビザーが新しい治療選択肢として承認され、AHAの患者さんに貢献できることを誇りに思っています」と述べています。