酸化的リン酸化と異所性骨化を関連を解明、進行性骨化性線維異形成症の新たな治療法の開発が期待
京都大学iPS細胞研究所(CiRA)は3月11日、難治性遺伝性疾患である進行性骨化性線維異形成症(FOP)における異所性骨化に酸化的リン酸化(OXPHOS)が深く関与しており、酸化的リン酸化の抑制が新しい治療法に繋がることを明らかにしたと発表しました。
進行性骨化性線維異形成症(FOP)は、全身の筋肉やその周りの膜、腱、靭帯などの通常は骨が形成されない部分が徐々に硬くなって骨になり、手足の関節の可動域が狭くなったり、背中が変形したりする遺伝性の疾患です。原因遺伝子は、骨形成因子(BMP)の受容体であるACVR1遺伝子です。
これまで、同研究グループは、進行性骨化性線維異形成症(FOP)患者さん由来のiPS細胞から誘導した間葉系幹細胞(MSC)を活用し、Activin AがmTORC1を活性化することで間葉系幹細胞(MSC)を軟骨細胞に分化させ、異所性骨化を引き起こすことが明らかになっていましたが、活性化されたmTORC1の下流で、どのようなシグナルが異所性骨化に関与しているのかは不明でした。
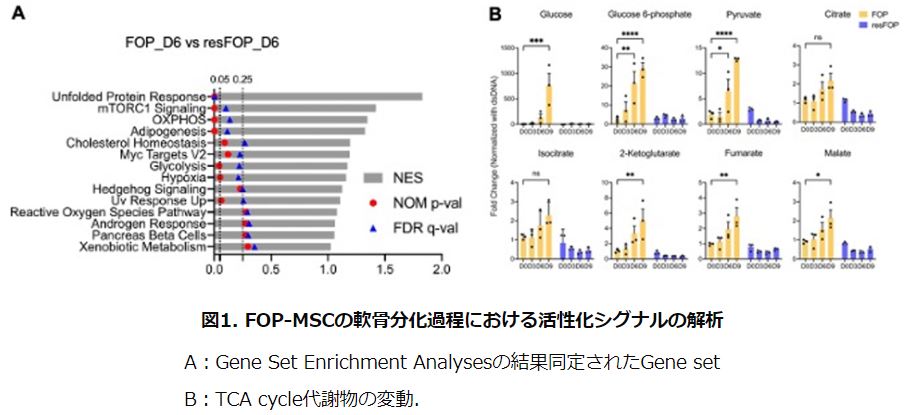
そこで今回、研究グループは、 進行性骨化性線維異形成症(FOP)の患者さん由来の間葉系幹細胞(FOP-MSC)とACVR1遺伝子を修復した間葉系幹細胞(resFOP-MSC)におけるActivin Aによる軟骨分化の過程の遺伝子発現を比較しました。
その結果、mTORC1シグナルと共に酸化的リン酸化シグナルが活性化していることが判明しました。
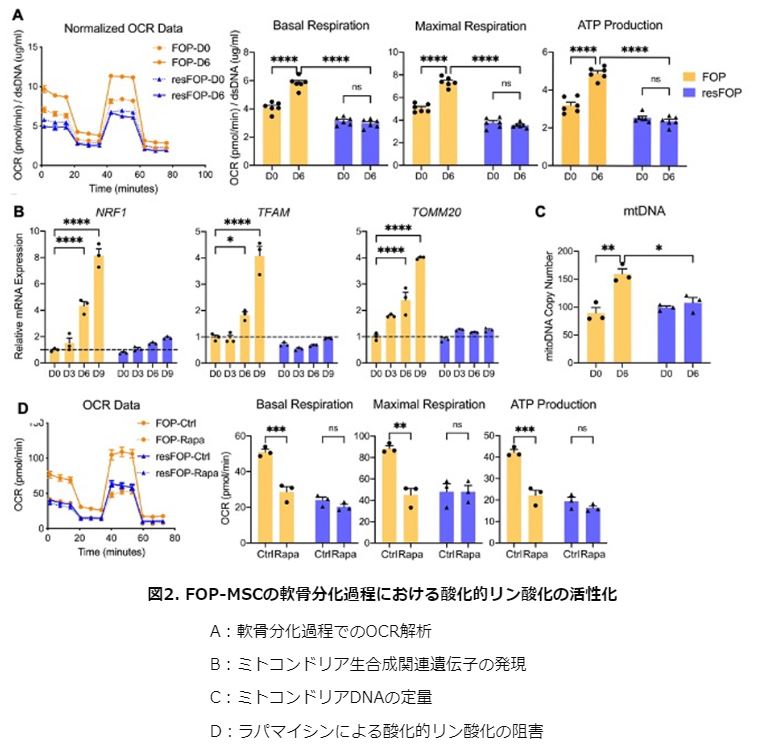
次に、酸素消費速度(OCR)を測定したところ、ATP産生量が増加しており、ミトコンドリア合成に関連する遺伝子(NRF1、TFAM、T OMM20)の発現も亢進し、ミトコンドリアDNA量も増加していました。mTORC1阻害剤であるラパマイシンがミトコンドリアの活性化を阻害していることから、酸化的リン酸化が活性化されていることが明らかになりました。
さらに、酸化的リン酸化阻害剤を軟骨分化実験に添加し、酸化的リン酸化の軟骨分化への関与を解析しました。その結果、Activin Aによる軟骨分化誘導に酸化的リン酸化の活性化が必要であることが判明しました。
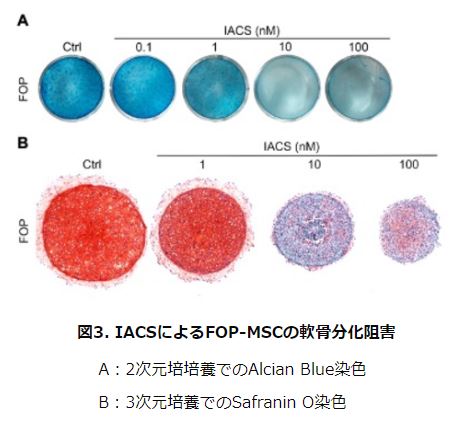
そこで、ヒト変異ACVR1遺伝子を導入した進行性骨化性線維異形成症(FOP)のモデルマウスを用いた外傷による異所性骨化誘導実験した結果、酸化的リン酸化阻害剤により初期の軟骨分化の過程が阻害されることが明らかになりました。
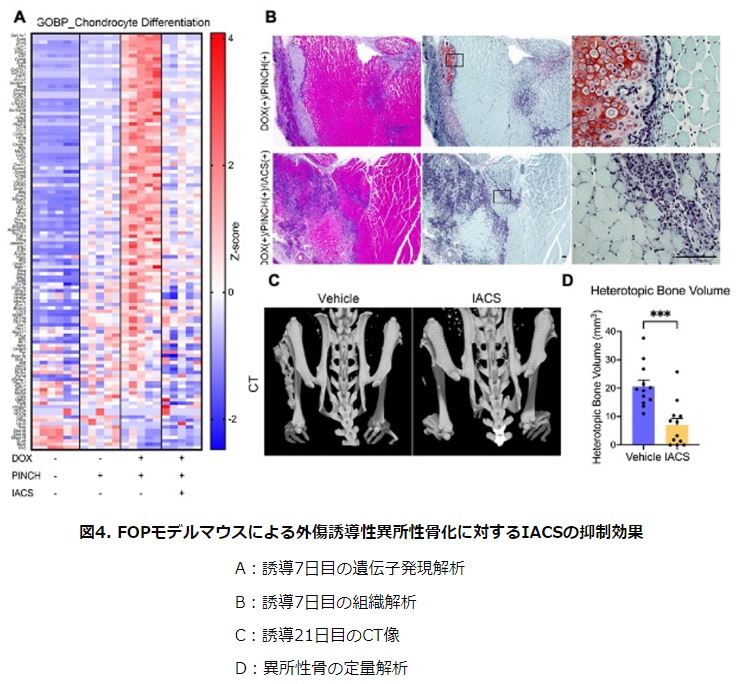
また、進行性骨化性線維異形成症(FOP)の異所性骨化の起源となるFibro/adipogenic progenitor(FAP)細胞の酸化的リン酸化を抑制することで、軟骨分化そして異所性骨化を抑制することが明らかになりました。
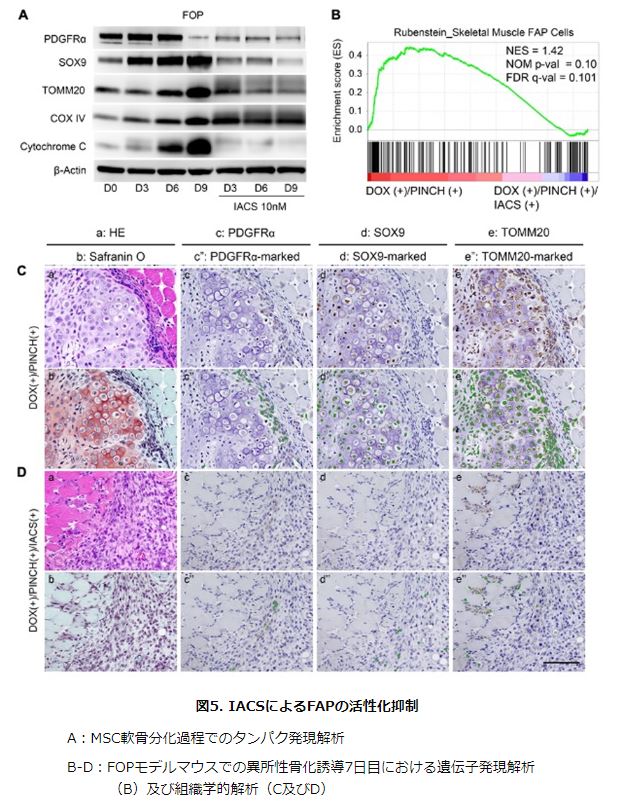
以上の研究成果より、進行性骨化性線維異形成症(FOP)の異所性骨化の発生機構の理解に繋がること、また、酸化的リン酸化が進行性骨化性線維異形成症(FOP)の新たな治療開発に繋がることが期待できるといいます。
京都大学iPS細胞研究所(CiRA)は「今回の実験で使用した酸化的リン酸化阻害剤は、抗がん剤としての臨床応用が検討されている薬剤でありFOP患者さんに対する長期間の服用は困難と考えられますが、フレアアップ時での短期間の使用等により、異所性骨化の初期の段階を抑制する治療薬としての有用性はあると考えられます。今後は他の候補治療薬との併用などの応用も考慮して開発が進められることが期待されます」と述べています。
なお、同研究の成果は、『Life Science Alliance』オンライン版に2月16日付で掲載されました。