脊髄性筋萎縮症(SMA)における骨格筋病変の発症メカニズムの一端を解明
京都大学iPS細胞研究所(CiRA)は1月17日、脊髄性筋萎縮症に関わるタンパク質「SMN」が骨格筋分化過程でMYOD-miRNA経路を制御することで、ミトコンドリアの機能的成熟を促進することを明らかにしたと発表しました。
この成果は、同研究所の池中亮裕研究員、齋藤潤教授らの研究グループによるもので、国際科学誌「Life Science Alliance」に1月5日付で掲載されました。
脊髄性筋萎縮症(SMA)は、脊髄の運動神経細胞の病変により、手や足などの筋肉が弱くなっていく疾患です。脊髄性筋萎縮症には、I型からIV型に分類されています。現在はゾルゲンスマ(一般名:オナセムノゲン アベパルボベク)などの遺伝子標的治療薬によって患者さんの予後が改善されつつありますが、最重症型のI型に対する効果は限定的であり、引き続き新たな治療の開発が必要とされています。
これまで、SMAは運動神経の疾患と考えられおり、運動神経におけるSMNの機能が解析されていました。一方、近年ではミトコンドリアの機能異常を含む骨格筋固有の病変も報告されていることから、SMAの新たな治療標的として骨格筋が注目されています。しかし、SMAにおける骨格筋病変の発症機序は解明されていません。そこで今回の研究では、脊髄性筋萎縮症の患者さんから樹立したiPS細胞とマウス由来筋芽細胞を用い、SMAにおける骨格筋病変の発症機序を調べたそうです。
その結果、SMNを欠損した骨格筋細胞では、ミトコンドリアの成熟に重要なマイクロRNA(miRNA)である「miR-1」および「miR-206」の発現量が低下していることが判明。miR-1およびmiR-206の転写開始点の上流で、SMNが転写因子「MYOD1」と共に結合しており、それらの転写活性に対する制御への関与が示唆されました。
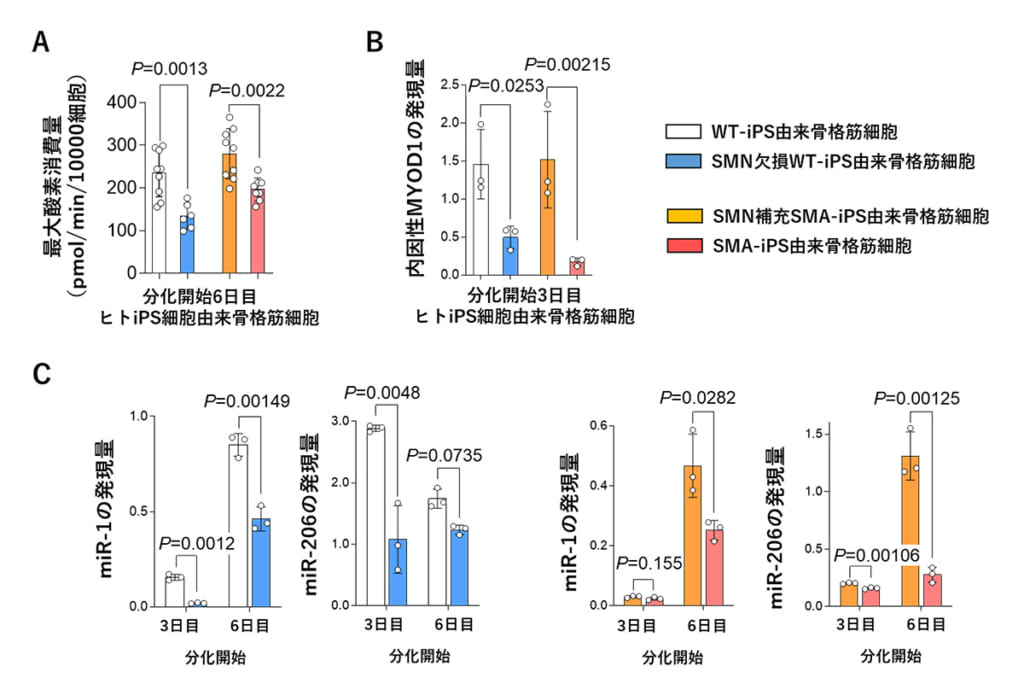
さらに、miR-1とmiR-206を補充したところ、脊髄性筋萎縮症モデルマウス由来筋管細胞の疾患表現型を改善したことから、これらの因子が治療標的として有望であることが示されたといいます。
今回の成果について、研究グループはプレスリリースにて、「本研究は、SMAの骨格筋病変の発症機構の1つを明らかにしました。今後、骨格筋を標的とした新規治療法の開発に繋がることが期待されます」と述べています。