iPS細胞活用でパーキンソン病の誘引物質早期検出に成功
慶応義塾大学医学部をはじめとする研究グループはiPS細胞から神経細胞を作製する技術を用いて、パーキンソン病(指定難病6)誘引物質の早期検出に成功しました。従来は1ヶ月以上かかる神経細胞の製作を1週間で可能にし、細胞分化後10日程度でパーキンソン病に関わる因子を検出しました。今回の技術を用いて新たな創薬開発のスピード向上が期待されます。
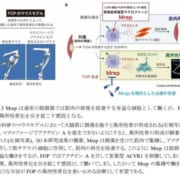
パーキンソン病は手の震えや筋肉のこわばり、転びやすさなど、運動に関わる症状があらわれる難病です。高齢者に見られることがおおく、特に65歳以上では100人に1人が罹患します。発症にはドーパミンが関与していることが知られており、中脳にある黒質神経細胞(ドーパミン神経)にαシヌクレインが凝集することが関与していると考えられています。研究グループはパーキンソン病を併発しやすいとされるゴーシェ病に着目し、Ⅰ型ゴーシェ病患者由来のiPS細胞から神経細胞を作製し、糖脂質の蓄積とαシヌクレインの関連性を調査しました。ゴーシェ病は先天性の代謝異常疾患であり、特にⅠ型に分類されるゴーシェ病は高齢になるとパーキンソン病になるリスクが9~14%になります。これには脳内の糖脂質蓄積が関与していると考えられていますが、詳細は明らかになっていません。
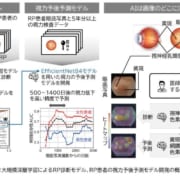
研究グループは以前、iPS細胞から神経細胞を効率よく作成する分化誘導技術を開発しました。転写因子をコードした合成mRNAを導入し神経分化を促進でき、この技術を用いると通常1ヶ月以上かかる分化誘導を1週間程度で行える利点があります。この技術を用いてゴーシェ病患者由来のiPS細胞からドーパミン神経へ分化誘導しました。その結果、従来の方法では60日間以上かかる糖脂質の蓄積を、わずか10日で確認できました。さらに、この時点でαシヌクレインの凝集は未確認だったものの、αシヌクレインのリン酸化修飾が更新され神経変性しやすい状態であることがわかりました。また、糖脂質の分解を促す遺伝子を強制発現させるとαシヌクレインの凝集が抑制されました。