活性化PI3Kδ症候群(APDS)治療薬ジョエンジャ錠、日本で製造販売承認を取得
株式会社オーファンパシフィックとPharmingグループは3月24日、選択的PI3Kδ阻害剤「ジョエンジャ錠70mg」「ジョエンジャ錠30mg」「ジョエンジャ錠10mg」(一般名:レニオリシブ、leniolisib)について、成人及び4歳以上の小児の活性化PI3Kδ症候群(APDS)を効能又は効果とした製造販売承認をオーファンパシフィックが2026年3月23日付で取得したと発表しました。
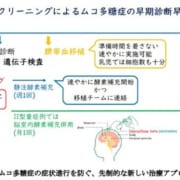
活性化PI3Kδ症候群(APDS)は、体内の免疫細胞の発達と機能に不可欠な遺伝子の変異によって引き起こされる、まれな遺伝性の原発性免疫不全症です。世界で100万人に1人から2人が罹患するとされています。重度かつ反復性の副鼻腔や肺の感染症、気管支拡張症、自己免疫性合併症など幅広い症状が現れることが特徴です。他の疾患と症状が共通しているため診断が難しく、診断までに中央値で7年を要することが報告されています。進行性の疾患であるため、診断が遅れることで経時的に傷害が蓄積し、不可逆的な肺損傷やリンパ腫などが生じる恐れがあります。
ジョエンジャ錠は、活性化PI3Kδ症候群(APDS)の原因となる経路を選択的に阻害することで、同疾患の治療や病状のコントロールの改善に寄与することが期待される薬です。同剤は、米国、英国、オーストラリア、およびイスラエルにおいて、成人および12歳以上の小児患者さんにおける活性化PI3Kδ症候群(APDS)に対する唯一の治療薬として承認されており、日本においては2023年5月に希少疾病用医薬品の指定を受けていました。
オーファンパシフィックはプレスリリースにて、「本邦のAPDS患者さんとそのご家族、そして患者さんを支える医療関係者の皆様に本剤を一日も早くお届けできるよう、Pharmingグループと協力して安定供給と適正使用の推進に努めてまいります」と述べています。