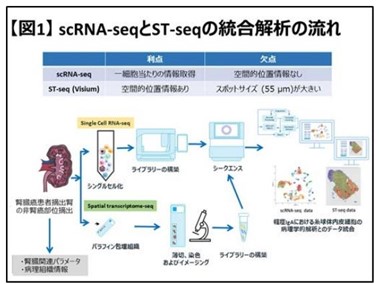
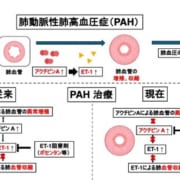
先天性血栓性血小板減少性紫斑病に対するADAMTS-13、製造販売承認を申請
武田薬品工業株式会社は8月17日、ADAMTS-13(遺伝子組換え)(開発コード:TAK-755)について、先天性血栓性血小板減少性紫斑病(cTTP)を予定される効能または効果として厚生労働省に対し、8月16日付で製造販売承認申請を行ったと発表しました。
先天性血栓性血小板減少性紫斑病(cTTP)は、フォン・ヴィレブランド因子(VWF)切断プロテイナーゼであるADAMTS13の欠乏により生じる希少な慢性かつ消耗性の血液凝固障害である血栓性血小板減少性紫斑病(TTP)の1つです。血小板減少症と溶血性貧血などの症状を特徴とします。これまでに、先天性血栓性血小板減少性紫斑病(cTTP)の治療薬として承認された薬剤はなく、急性症状の治療や予防には新鮮凍結血漿が用いられます。
今回の製造販売承認申請は、主に日本人5名を含む先天性血栓性血小板減少性紫斑病(cTTP)の患者さんを対象としたグローバル臨床第3相試験である281102試験および臨床第3b相継続試験であるTAK-755-3002試験の中間解析結果に基づくものです。これらの試験において、ADAMTS-13(遺伝子組換え)は先天性血栓性血小板減少性紫斑病(cTTP)の治療薬として有効性および安全性が認められました。
今回、製造販売承認申請を行ったADAMTS-13(遺伝子組換え)は、血栓性血小板減少性紫斑病(TTP)を対象とした初めての遺伝子組換えADAMTS13製剤であり、先天性血栓性血小板減少性紫斑病(cTTP)の治療薬として製造販売承認申請を行いました。また、後天性(免疫性)血栓性血小板減少性紫斑病(iTTP)の治療薬としても全世界で開発を進めているそうです。