ハッチンソン・ギルフォード症候群、エメリー・ドレイフス型筋ジストロフィーなどの新規治療法開発に繋がる核膜の損傷修復に関わるメカニズムを発見
広島大学は7月11日、核膜の損傷修復に関わる新たなメカニズムを発見し、さまざまなタイプの細胞を物理的ストレスにさらし核膜損傷を誘導した結果、細胞増殖を抑制するタンパク質p21がDNA損傷や細胞死と関連していること、p21の量を操作することで、核膜の損傷により誘導されるDNA損傷や細胞死の制御に成功したと発表しました。
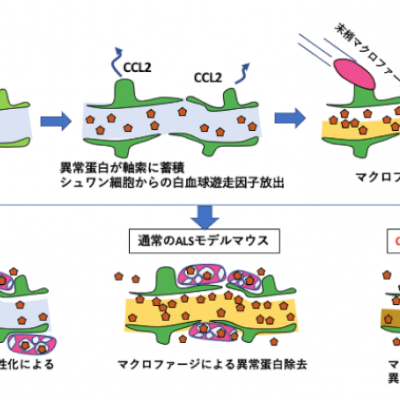
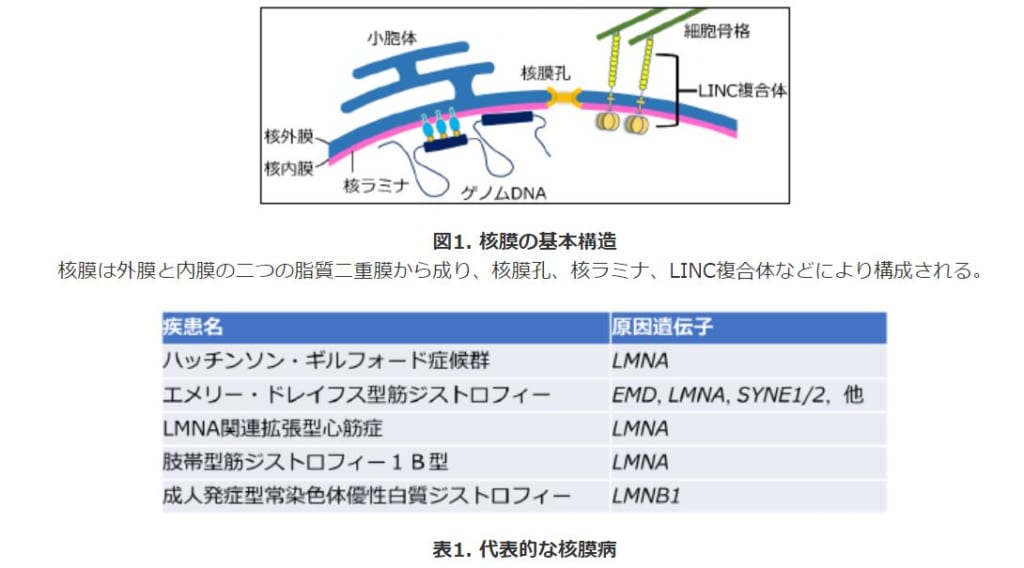
核膜は内膜と外膜と呼ばれる2つからなり、その中に遺伝情報を担うDNAを収納し、保護しています。近年、核膜が頻繁に損傷と修復を繰り返すこと、核膜の損傷がDNA損傷や細胞死を引き起こすことが明らかとなっています。そして、そのような障害は、致死性の早老症であるハッチンソン・ギルフォード症候群や筋ジストロフィーの一種であるエメリー・ドレイフス型筋ジストロフィーに代表される核膜病に加え、固形がんなど、さまざまな疾患と関連があると報告されています。特に、核膜病は特定の組織に強く症状が現れることから、細胞のタイプにより核膜損傷による影響に違いがあると考えられていましたが、違いが生じる要因は明らかになっていませんでした。
そこで今回、さまざまなタイプの細胞において人工的に核膜を損傷させ、その影響を比較するという研究が行われました。その結果、膠芽腫に由来する細胞の一部では、核膜損傷によりDNA損傷と細胞死が誘導され、p21というタンパク質の発現量が障害と関連していることを突き止めました。さらに、p21の発現量を減少させると損傷に対する感受性が高まり、逆にp21発現量を増大させると感受性が低下することも分かりました。また、核膜損傷に対して感受性の高い細胞の一部では、核膜の損傷修復に異常を来たすことも明らかになりました。
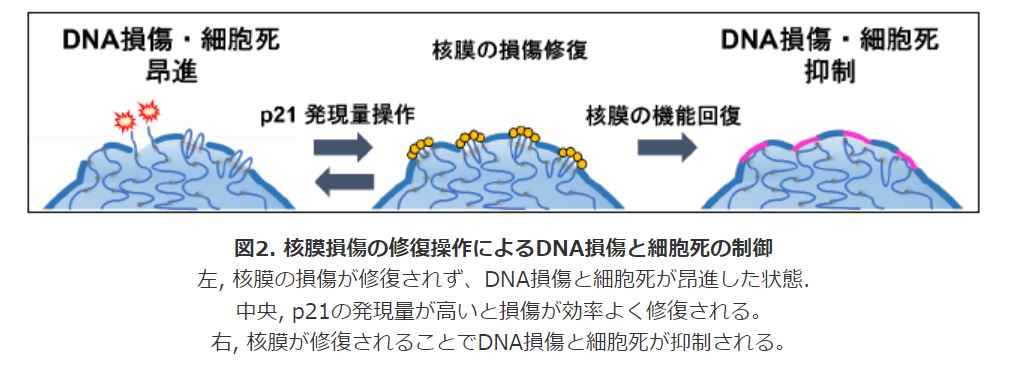
今回、p21の発現量を操作することで核膜損傷によるDNA損傷や細胞死を制御できることが証明されました。現在、核膜病の根治的な治療法は存在しませんが、今後、さらなる研究が進み、核膜の修復メカニズムの解明がされ、p21やその他の核膜修復の鍵となる分子の量・機能を改善することが可能となれば、核膜修復の促進による核膜病の新規治療法の開発に繋がると期待できます。
また、逆に核膜修復を阻害することにより、細胞死を誘導し抗腫瘍効果が得られると予想できます。今回の研究で用いた膠芽腫においても、核膜修復を阻害する方法の確立が、新規治療法開発に繋がることが期待できます。
なお、同研究の成果は、英国Nature Publishing Groupのオンライン誌「Cell Death Discovery」に、7月8日付で掲載されました。