ミトコンドリア心筋症の進行メカニズムの一端を解明
国立循環器病研究センターは4月22日、大阪大学、京都大学、九州大学、北海道大学、順天堂大学、埼玉医科大学、メルボルン大学との共同研究により、ミトコンドリア心筋症の病態進行過程で「転写因子Atf3が重要な運命決定因子として機能する」ことを明らかにしたと発表しました。
ミトコンドリアは、細胞のエネルギー産生を担う重要な器官です。ミトコンドリア病(指定難病21)は、ミトコンドリアの機能不全を引き起こす遺伝子の変異によって発症し、全身のさまざまな臓器に障害をもたらす可能性があります。特に心臓の機能が低下し、血液を全身に送ることがしづらくなるミトコンドリア心筋症は、患者さんの予後を大きく左右することが知られています。しかし、その進行メカニズムは未解明な点が多く、有効な治療法が確立されていません。
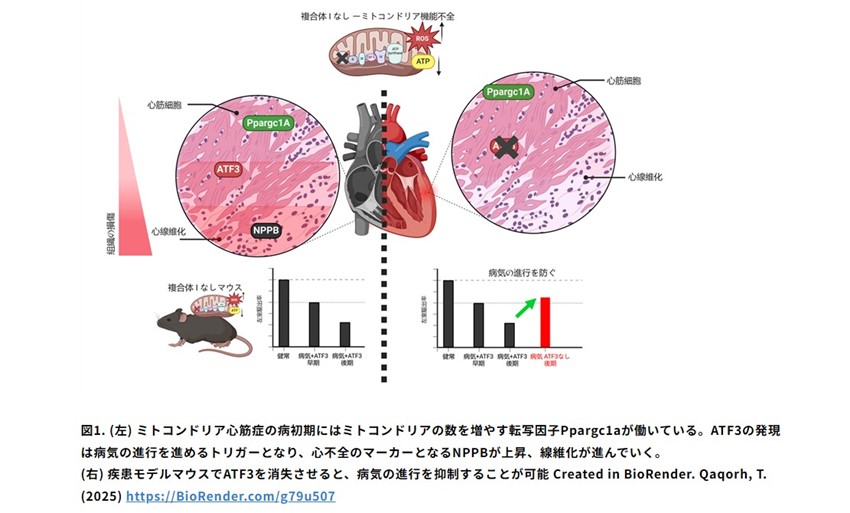
今回、研究グループは、国立循環器病研究センターで治療を受けたミトコンドリア心筋症の8ヶ月齢の女児の心筋組織を詳細に解析。その結果、重症化した心筋組織の中に、比較的変性の少ない部分と進行した部分が混在していることを発見しました。遺伝子発現解析を行ったところ、心不全の指標となる遺伝子NPPBは、変性の進行した部分で強く発現していました。一方、比較的正常な部分では、転写因子ATF3が多く発現していることが明らかになりました。さらに、患者さんの細胞を用いた単一細胞レベルの遺伝子発現解析から、ATF3の発現上昇とともに、ミトコンドリアの数を増やす働きを持つPPARGC1Aの発現が低下し、NPPBを発現する不全心筋へと移行する可能性が示唆されました。

次に、ヒトのミトコンドリア心筋症患者さんで見出された知見を検証するため、ミトコンドリア心筋症のモデルマウス(FS6KDマウス)を用いて解析を行いました。病初期のモデルマウスの心臓では、Ppargc1aを強く発現する心筋細胞が多く見られましたが、一部ではすでにNppbを発現する細胞も存在し、組織の不均一性が確認されました。詳細な単一細胞遺伝子発現解析により、病態の進行期にAtf3の発現が一過的に上昇することが明らかになりました。さらに、Atf3を遺伝的に欠損させたモデルマウスでは、心機能の低下が抑制されることが確認され、Atf3が病態進行を促進する重要な因子であることが示唆されました。
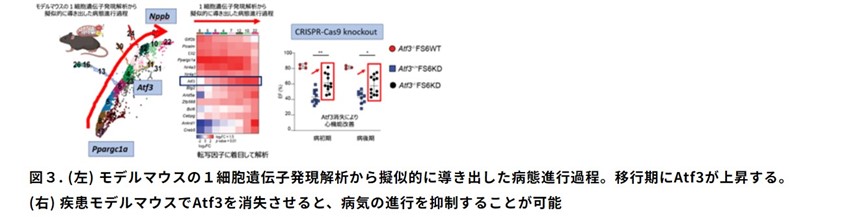
以上の研究成果より、これまで均一であると考えられていた末期心不全のミトコンドリア心筋症の心筋組織においても、進行度の異なる細胞が混在している可能性が示唆されました。これは、治療の介入によって改善が見込める心筋細胞が残存している可能性を示唆するものであり、今後の新たな診断法や治療法の開発につながることが期待されます。研究グループは今後、ミトコンドリア心筋症、ミトコンドリア病のより詳細な病態解明と、それに基づいた新しい治療法の開発を目指していくとしています。











