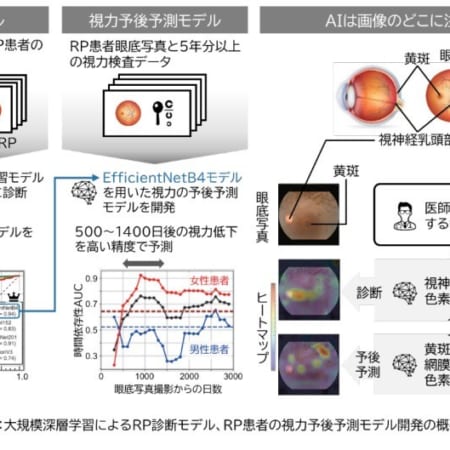
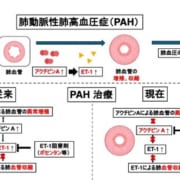
mRNA医薬を用いてデュシェンヌ型筋ジストロフィー(DMD)モデルマウスの治療に成功
東京科学大学は3月25日、同大と国立精神・神経医療研究センター(NCNP)ならびに札幌医科大学の研究チームがmRNA医薬を用いて、難治性筋疾患であるデュシェンヌ型筋ジストロフィー(DMD)の治療に成功したと発表しました。
デュシェンヌ型筋ジストロフィー(DMD)は、筋肉の構造維持に関与するジストロフィンというタンパク質が作られないため、筋組織の破壊や筋力低下が徐々に進行する遺伝性疾患です。現在、根治的な治療法は存在せず、理学療法、装具、矯正手術などの対症療法が主流となっています。
近年、変異を生じているジストロフィン遺伝子に対するアンチセンス核酸を用いたエクソン・スキップ療法が開発され、日本初の核酸医薬品であるビルトラルセンとして条件付き承認を受けました。しかし、エクソン・スキップ療法には、効果が特定の遺伝子変異に限定されるため、治療対象が限定されるという課題があります。
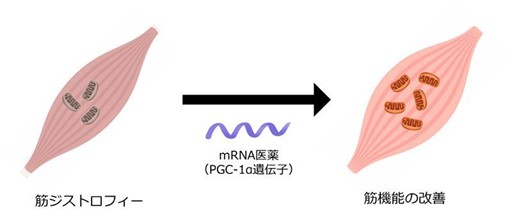
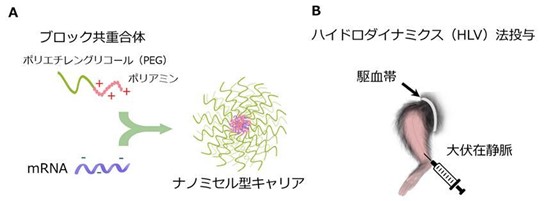
今回、デュシェンヌ型筋ジストロフィー(DMD)の筋症状を改善させる治療用タンパク質として、ミトコンドリアの合成や代謝活性を高める働きを持つタンパク質PGC-1αを用いて研究を行いました。さらに、mRNAを標的の筋組織に広く投与する手法として、研究グループが独自に開発を進めてきた「ナノミセル型mRNAキャリア」を用い、ハイドロダイナミクス(HLV)法投与を実施。ナノミセル型キャリアを用いたHLV法では、炎症をほとんど引き起こすことなく、mRNAを標的の筋細胞に広範囲に届けることが可能だといいます。
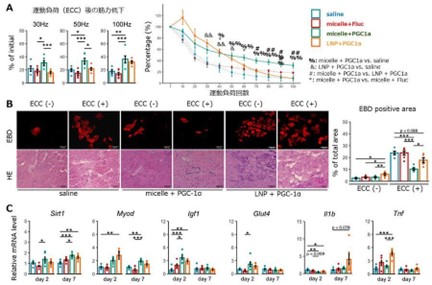
今回の研究では、デュシェンヌ型筋ジストロフィー(DMD)疾患モデルマウス(mdxマウス)および野生型マウスを用いて筋機能計測を行い、mdxマウスは過度の運動負荷により筋力が著しく低下し、顕著な組織傷害が見られるなど、デュシェンヌ型筋ジストロフィー(DMD)の病態を反映していることを確認しました。一方、PGC-1α mRNAをナノミセル型キャリアに内包し、HLV法で投与したデュシェンヌ型筋ジストロフィー(DMD)マウスを投与1週間後に評価した結果、生食投与群やコントロールmRNA投与群と比較して、運動誘発性の筋力低下が生じにくくなることが確認されました。加えて、運動負荷後の筋組織傷害も有意に低下しました。投与後の筋組織の遺伝子発現解析の結果、ミトコンドリア活性の指標であるSirt1などの遺伝子群、筋活動に関連する遺伝子群(MyoD、Glut4など)、および筋肥大に関与する遺伝子(IGF-1など)の発現が増加していました。これにより、PGC-1α mRNAの投与が細胞内シグナルを活性化し、筋症状改善につながったと考えられるといいます。
以上の研究成果より、mRNAを疾患治療用医薬品として活用する新たな可能性が示されました。日本発の新しい難治疾患治療法の開発が進み、難治性疾患に苦しむ患者さんの治療選択肢を広げる大きな一歩となることが期待されます。
なお、同研究の成果は、「Advanced Science」に3月6日付で掲載されました。