デュシェンヌ型筋ジストロフィー治療薬ビルテプソ、長期有効性・安全性データが学術誌に掲載
日本新薬株式会社は5月31日、デュシェンヌ型筋ジストロフィー(DMD)治療剤「ビルテプソ(R)」(一般名:ビルトラルセン)の米国第II相非盲検継続投与試験における長期有効性および安全性データ(109週時点での中間解析結果)が、学術誌「Journal of Neuromuscular Diseases」に掲載されたことをお知らせしました。
デュシェンヌ型筋ジストロフィー(DMD)は、ジストロフィンタンパク質の欠損が原因で骨格筋や心筋、肺の筋力低下を引き起こす進行性の筋ジストロフィー。DMDにはさまざまな遺伝子変異型があり、同剤の投与対象は、エクソン53スキッピングにより治療可能な遺伝子変異が確認されたDMDです。
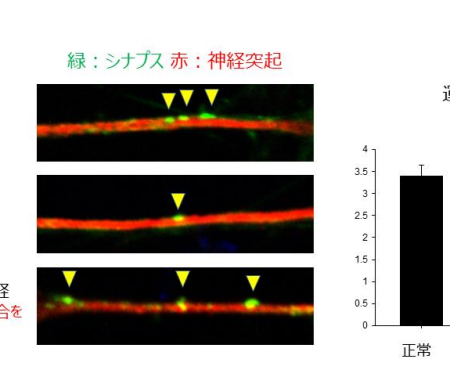
今回、同誌に掲載されたデータは、北米で実施された第II相試験の継続投与試験の結果から得られたものであり、学会等での発表は終えているそうです。同試験では、長期間の運動機能および安全性を評価するために、24週間の試験を終了した後もエクソン53スキッピングにより治療可能なジストロフィン遺伝子の欠失が確認されていている4~10歳未満のDMD患者さん16例全員が、継続投与に登録されているといいます。同試験では、床からの立ち上がり時間、10m歩行/走行時間、6分間歩行距離を運動機能を評価項目として、患者背景を一致させた自然歴データを対照群として比較しています。
日本新薬はプレスリリースにて「この第II相非盲検継続投与試験に加え、第III相試験(RACER53 試験)を行っており、ビルテプソの有効性および安全性を検証していきます」と述べています。
なお、ビルテプソについては、エクソン53スキッピングにより治療可能なジストロフィン遺伝子の欠失が確認されているデュシェンヌ型筋ジストロフィー患者の治療薬として、日本国内では条件付早期承認制度の対象医薬品となり2020年3月に厚生労働省から承認され、同年5月から販売および情報提供活動が行われています。