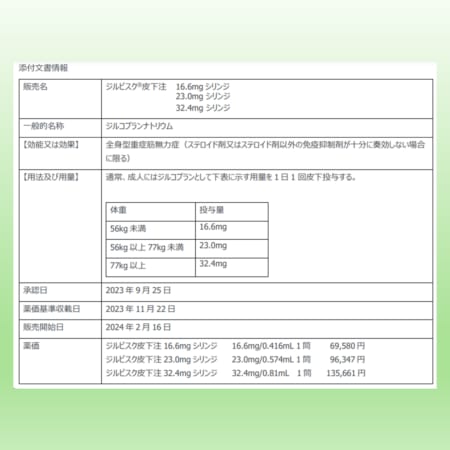
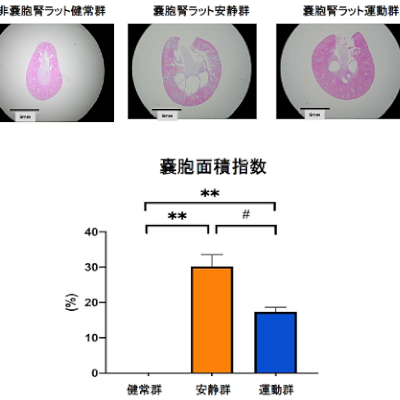
ビルトラルセン国内P1/2試験結果、世界筋学会で発表 日本新薬の筋ジス薬 海外P2試験も
日本新薬は3日、アルゼンチンで開催中の世界筋学会で、デュシェンヌ型筋ジストロフィー治療薬ビルトラルセン(開発コード=NS-065/NCNP-01)の日本での臨床第1/2相(P1/2)試験結果と、米国… この記事は会員限定です。会員登録すると最後までお読みいただけます。
RareS.コメント
エクソンスキップ作用を持つ、デュシェンヌ型筋ジストロフィー治療薬ビルトラルセン(開発コード=NS-065/NCNP-01)の日本での臨床第1/2相試験結果と、米国とカナダでのP2試験結果が公表されました。
デュシェンヌ型筋ジストロフィーは、指定難病である筋ジストロフィーの一種で、ジストロフィンタンパク質が遺伝子変異によりうまく作れないことを原因とした、男性に偏って生じる疾患です。主に筋力の低下などの症状を呈します。
日本での第1/2相試験では、24週間の投与で生じた副作用は軽度または中等度にとどまり、5歳から12歳までの男児16人中14人で必要なジストロフィンタンパク質の増加と身体的運動機能の低下を確認できました。また、カナダでの試験では、24週間の投与で16人中16人がジストロフィンタンパク質の増加が見られ、タイムドテスト(特定の運動に要する時間の測定による運動機能の検査)による改善が見られました。
この薬は、日本において先駆け審査指定制度という、命に関わるにも関わらず有効な治療薬がない疾患に対し、日本で世界に先駆けて実用化するための制度の指定を受けており、普通の薬剤よりも早く発売されることが見込まれます。注目していきたいですね。
日本における臨床試験のリリース情報です。(英語のみ)日本の臨床試験結果
カナダにおいての臨床試験のリリース情報です。(英語のみ)カナダの臨床試験結果