筋萎縮性側索硬化症(ALS)発症を抑える「防御役」であるRNAの機能が判明
東北大学は11月5日、筋萎縮性側索硬化症(ALS)の原因タンパク質が細胞内で異常に固まるのを、細胞内に豊富に存在するRNAがどのように防いでいるのかを明らかにしたと発表しました。
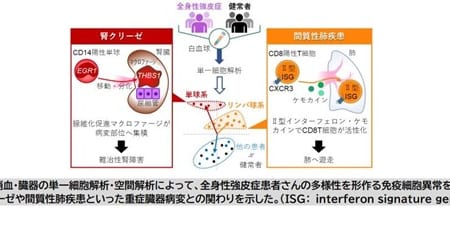
筋萎縮性側索硬化症(指定難病2、ALS)は、運動神経細胞が機能を失うことで呼吸や手足の運動が困難になる、進行性かつ致死性の神経変性疾患であり、根本的な治療法はまだ確立していません。筋萎縮性側索硬化症(ALS)は、Fused in sarcoma(FUS)などといった特定のタンパク質が神経細胞内で異常に凝集し、障害を引き起こすことで発症すると考えられています。近年、このタンパク質の異常凝集は、「液-液相分離(LLPS)」という現象によって形成される、タンパク質が高濃度に集まった液体状態(液滴)を経由して生じることが提案されています。細胞内には多量のRNAが存在しますが、このRNAが液滴の形成や安定性を調整していることは知られていたものの、具体的にどのような仕組みで制御しているかは不明でした。
今回、研究グループは、分子の状態をそのまま観察できるラマン顕微鏡を用いて、筋萎縮性側索硬化症(ALS)原因タンパク質であるFUSとRNAの相互作用を詳しく調べました。その結果、RNAの「長さ」によって、FUSタンパク質の凝集に対する防御の働きが異なることが判明しました。
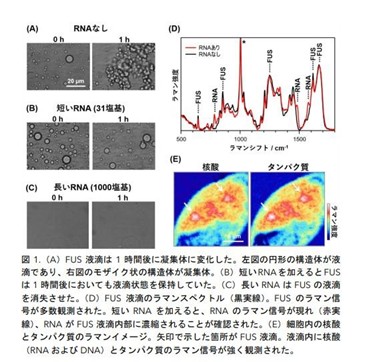
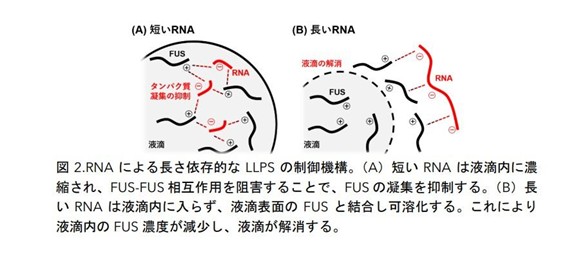
50塩基以下の短いRNAをFUS液滴に加えると、RNAの配列や構造に関係なく、液滴は安定して保たれ、凝集が抑えられました。短いRNAはFUSの液滴内部に自発的に濃縮され、FUS同士の接触を妨害する「バッファー」の役割を果たすことで凝集を抑制すると考えられます。
一方、1000塩基を超える長いRNAを加えると、液滴自体が消失しました。長いRNAは液滴内部には取り込まれず、液滴の界面にあるFUSと結合することでFUSの親水性を高め、液滴を解消させると考えられます。
さらに、生きた細胞に浸透圧ストレスを与えてFUS液滴を生成させた際、ラマン顕微鏡を用いて検討したところ、液滴がタンパク質のみではなく、多量の内在性RNAを濃縮して含んでいることを初めて明らかにしました。液滴の内部のRNA濃度は、外側の溶液よりも2~3倍程度高いことが定量されています。
以上の研究成果より、RNAが筋萎縮性側索硬化症(ALS)原因タンパク質であるFUSの液滴形成と凝集を、その長さに基づいて制御する「防御役」として働いていることが提案されました。研究グループは今後、筋萎縮性側索硬化症(ALS)以外の神経変性疾患(アルツハイマー病やパーキンソン病など)においても、RNAによる同様のLLPS制御機構が関与するかを検証し、有効な薬剤設計の指針の提示を目指すとしています。
なお、同研究の成果は、国際誌「JACS Au」に11月3日付で掲載されました。