家族性ALSに対するTofersenの臨床試験結果を公表
バイオジェン(アメリカ)は2020年7月8日(現地時間)、筋萎縮性側索硬化症(ALS 指定難病2)に対するTofersenの臨床第Ⅰ/Ⅱ相試験の結果が「ニューイングランド・ジャーナル・オブ・メディシン」に掲載されたと発表しました。Tofersenは家族性のALSのなかでも比較的患者数の多い、SOD1遺伝子に異常のあるタイプのALSの治療薬として注目されています。
家族性ALSの原因遺伝子としてのSOD1
ALSは、脳から発せられる、筋肉を動かす指令を伝える神経が障害され、身体が動かしづらくなり徐々に筋肉が瘦せていく疾患です。遺伝子の突然変異によって起こる孤発性ALSが大半ですが、全体の5%程度は遺伝性のある家族性ALSに分類されます。一部の家族性ALSの原因としてSOD1遺伝子の変異が特定されています。SOD1は体内で発生する有害な活性酸素を取り除く働きがある酵素で、SOD1遺伝子の変異により起こるALSは家族性ALSに多いことが明らかになっています。SOD1遺伝子に変異が起こるとSODの活性が下がるのではなく、異常な毒性を持つようになるために神経細胞死が引き起こされると考えられています。
SOD1-ALSに対するTofersenの有効性
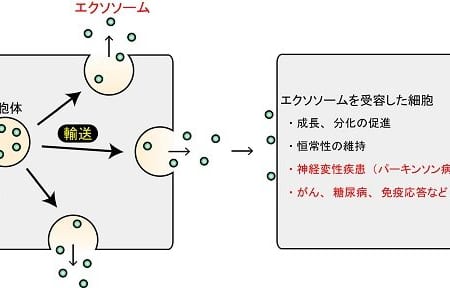
今回行われた試験は、スーパーオキサイドジスムターゼ1(SOD1)酵素を作り出す遺伝子に変異が起こるタイプのALS患者を対象に行われた、安全性および薬物動態などを評価する第Ⅰ/Ⅱ相試験です。反復漸増投与を受けたSOD1-ALS患者はTofersen (20 mg、 40 mg、 60 mg または 100 mg)、またはプラセボ薬を12週間投与されました。1回以上のTofersen投与を受けた患者のうち、頭痛、処置痛、腰椎穿刺後症候群、転倒などの副作用がみられました。TofersenはSOD1遺伝子に対応するように設計されたアンチセンス・オリゴヌクレオチドです。SOD1遺伝子より写し取られたメッセンジャーRNA(mRNA)に結合し分解を誘導します。臨床第Ⅲ相試験も現在継続中であり、SOD1-ALSの成人患者を対象に、有効性と安全性の評価が進められています。