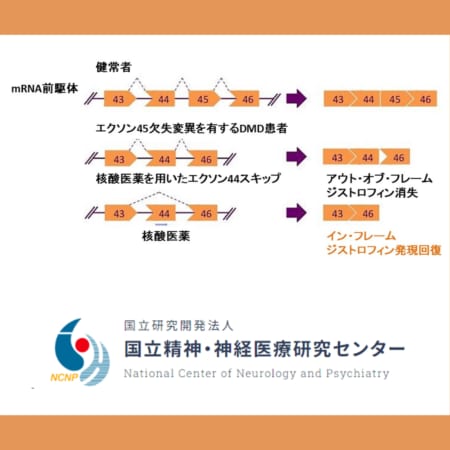
遺伝性難聴に対するゲノム編集技術を開発、内耳の異常タンパク質を修復し正常に機能させることに成功
順天堂大学は3月11日、東京大学との共同研究により、これまで根本的治療の存在しなかった遺伝性難聴に対して独自の遺伝子送達技術と遺伝子編集技術を組み合わせることにより患者内耳の遺伝子変異を効率よく修復し、内耳の異常タンパク質を修復する新技術を開発したと発表しました。
生まれつきの難聴には、130種以上の遺伝子の変異が原因で発症し、その最も大きな原因にGJB2(Gap Junction Protein Beta 2)と呼ばれる遺伝子の変異があります。GJB2は内耳の「ギャップ結合」と呼ばれるタンパク質の構成成分であり、内耳のイオン濃度を一定に保つ役割をしています。
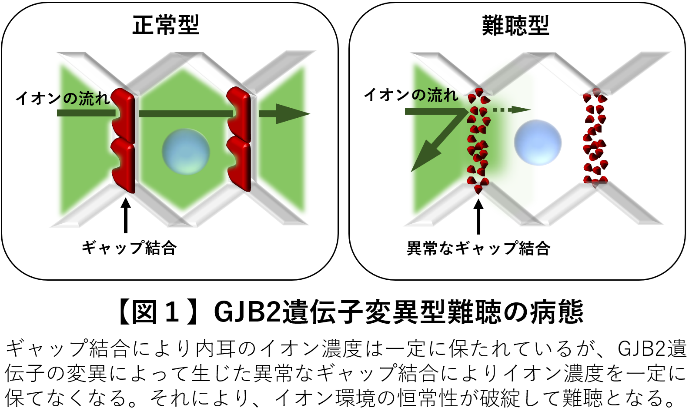
これまで、GJB2などの正常遺伝子を補充する治療の研究は進んでいましたが、顕性(優性)遺伝型と呼ばれる遺伝子変異のタイプでは遺伝子の補充は効果がなく、遺伝子情報を書き換えるゲノム編集の技術が必要とされていました。しかし、遺伝子の大きさや書き換えの効率など、技術的な困難によって有効な方法が開発されていませんでした。
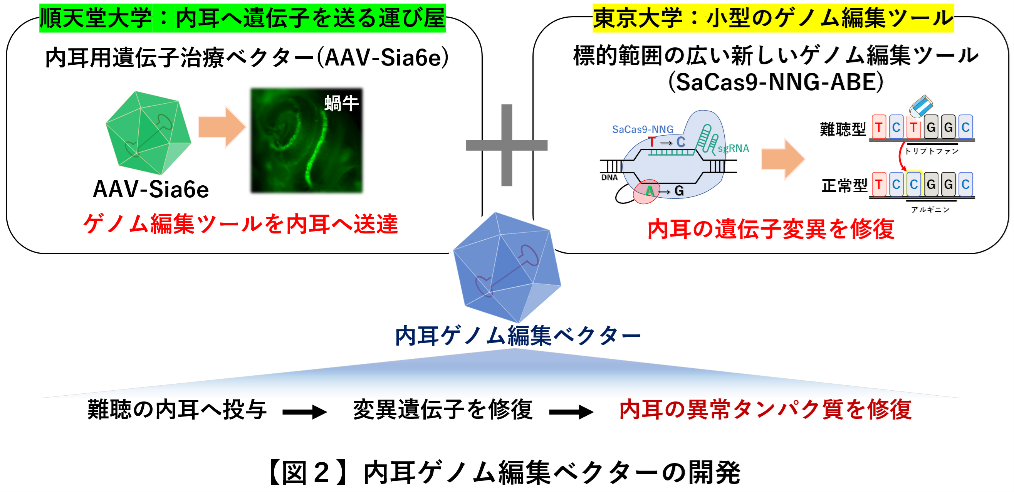
今回、研究チームは、遺伝子を内耳へ送り届けることができるアデノ随伴ウイルスベクター(AAV)と呼ばれる遺伝子の運び屋の「遺伝子治療ベクター」を遺伝子組み換えによって開発しました。しかし、AAVに搭載できる遺伝子のサイズに制限があるため、遺伝子サイズが大きい従来のゲノム編集ツールを1つの遺伝子治療ベクターだけで内耳に運ぶことは困難で、2つの遺伝子治療ベクターに分けて行う必要がありました。また、従来の方法では編集できる遺伝子の場所に制約があり、標的にできない遺伝子変異も多かったため、東京大学の研究チームは従来型のゲノム編集ツールよりも遺伝子サイズが小さく、標的範囲が広い新しいゲノム編集ツール「SaCas9-NNG-ABE」を開発。順天堂大学が開発した内耳へのAAVと東京大学で開発した最新のゲノム編集技術(SaCas9-NNG-ABE)を組み合わせた難聴への遺伝子治療技術により、GJB2と呼ばれる代表的な難聴遺伝子の変異箇所を効率よく書き換えて、内耳タンパク質の機能を正常に回復させる技術開発に初めて成功しました。
このベクターで顕性(優性)遺伝型のGJB2遺伝子変異型難聴 (GJB2 R75W)を持つモデル動物やモデル細胞に対するゲノム編集治療を実施したところ、一回の投与で標的とする遺伝子変異を効率よく修復し、疾患モデル細胞と難聴モデルマウスの両方でギャップ結合タンパク質の構造体に明らかな改善を認めました。さらに修復されたギャップ結合では本来の物質輸送能が回復していることを確認したといいます。
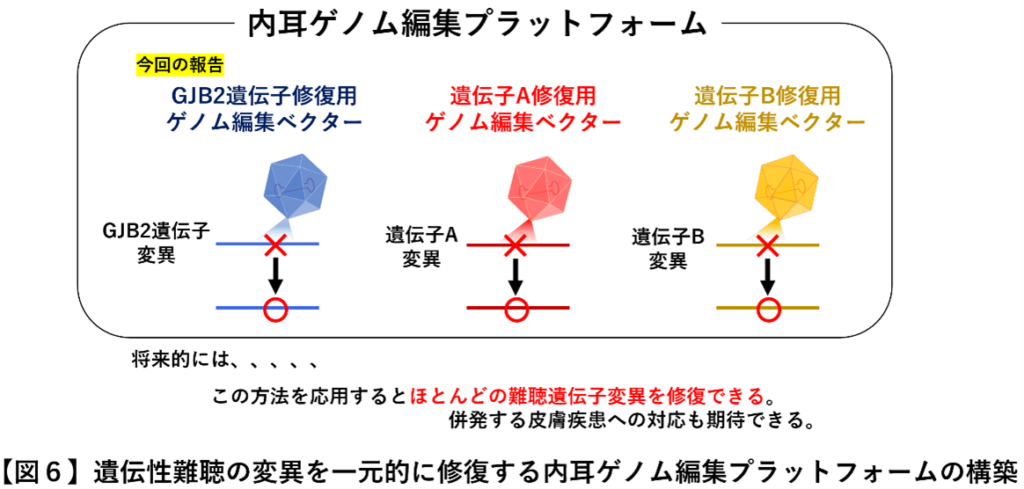
今回開発した内耳ゲノム編集ベクターは従来型では編集の困難であった遺伝子変異に対するゲノム編集も可能であるため、同技術を応用するとさまざまなタイプの難聴遺伝子変異型を修復することが可能になるといいます。近年では、生まれつきの難聴だけでなく、若年期に難聴を発症する、若年発症型両側性感音難聴(指定難病)の遺伝子変異も多く発見されていることから、今後は多種多様な原因遺伝子と変異型を有する遺伝性難聴に対し、それらを一元的に修復する内耳ゲノム編集プラットフォームを構築することが望まれます。また、今回対象としたGJB2 R75W変異は難聴だけでなく皮膚疾患を併発するため、将来的には皮膚疾患への適用にも期待されるといいます。
なお、同論文は、「JCI Insight」オンライン版に3月11日付で掲載されました。