慢性炎症性脱髄性多発根神経炎(CIDP)に対するヒフデュラの適応追加承認を申請
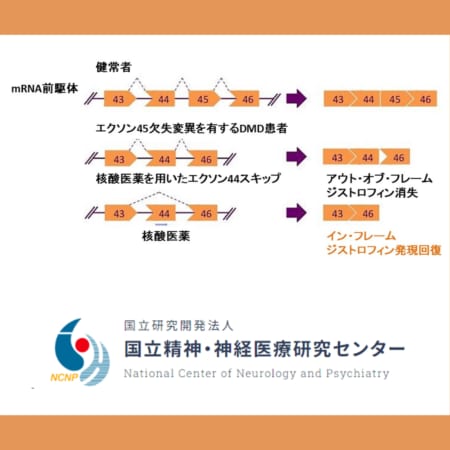
アルジェニクスジャパン株式会社は4月25日、抗胎児性Fc受容体(FcRn)抗体フラグメント・ヒアルロン酸分解酵素配合製剤「ヒフデュラ配合皮下注〔エフガルチギモド アルファ(遺伝子組換え)・ボルヒアルロニターゼ アルファ(遺伝子組換え)配合皮下注製剤〕」について、慢性炎症性脱髄性多発根神経炎(CIDP)に対する効能効果及び用法用量に関する製造販売承認事項一部変更承認の申請を提出したと発表しました。
慢性炎症性脱髄性多発根神経炎(指定難病14)は、末梢神経に炎症が起こり、運動障害・感覚障害が生じる疾患で、時間の経過とともに症状の悪化、再発と寛解を繰り返すことがあります。
ヒフデュラは、「ウィフガート点滴静注400mg〔エフガルチギモド アルファ(遺伝子組換え)点滴静注製剤〕」に、浸透促進剤ボルヒアルロニダーゼ アルファ(遺伝子組換え)を配合した固定用量の皮下投与製剤で、自宅などでの自己投与が可能な製剤です。今回の適応追加承認が申請されれば、エフガルチギモド(ウィフガート/ヒフデュラ)では、全身型重症筋無力症(gMG)、慢性特発性血小板減少性紫斑病(慢性ITP)に続き、日本国内において慢性炎症性脱髄性多発根神経炎(CIDP)が3つ目の適応症となります。
アルジェニクスジャパン代表取締役社長のヘルマン・ストレンガー氏は、今回の申請について、「この度、CIDPの適応追加承認の申請を提出できましたことを嬉しく思っております。治験に協力いただいた患者さんや医療従事者の皆様に深く感謝しております。CIDPは、末梢神経系の希少かつ重度な自己免疫疾患で、疲労感、四肢の筋力低下・感覚障害が生じることがあるため、生涯にわたり患者さんの生活に影響を及ぼします。CIDPの適応追加が承認されれば、CIDPの治療において、国内で最初のグロブリン製剤が承認されてから、25年ぶりのイノベーションになると言えます。できるだけ早く、ヒフデュラが新たな治療法を必要としているCIDP患者さんの治療に貢献できる日がくることを願っております」と述べています。
なお、ヒフデュラは、2024年3月に慢性炎症性脱髄性多発根神経炎(CIDP)の治療薬として、厚生労働省から希少疾病用医薬品として指定されています。