全身型重症筋無力症に対する皮下注射剤ジルビスクが初の自己注射可能な製剤として発売開始
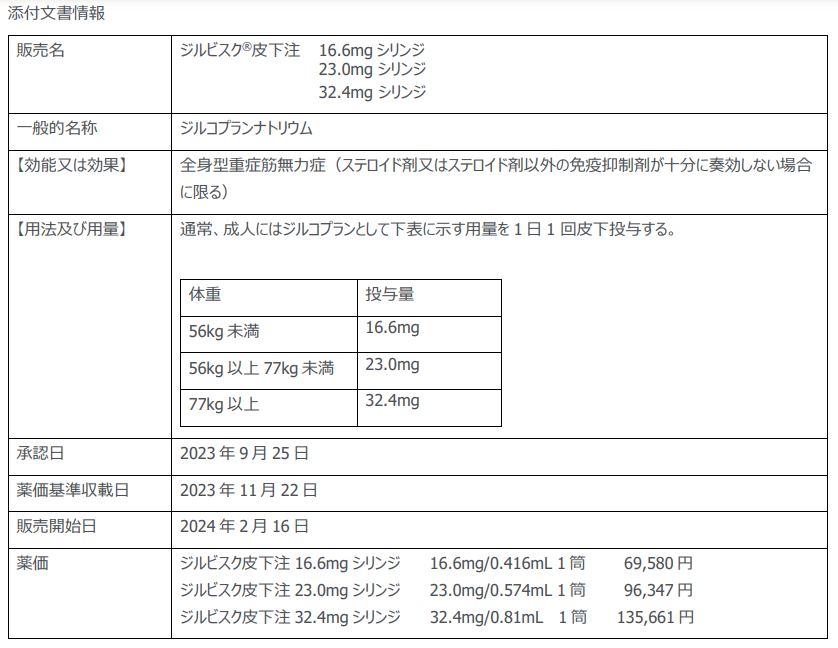
ユーシービージャパン株式会社は2月16日、補体(C5)阻害剤「ジルビスク皮下注16.6mg/23.0mg/32.4mgシリンジ」(一般名:ジルコプランナトリウム、以下ジルビスク)について、全身型重症筋無力症(ステロイド剤又はステロイド剤以外の免疫抑制剤が十分に奏効しない場合に限る)を効能・効果として、販売を開始したと発表しました。
全身型重症筋無力症(gMG)は、神経節接合部の機能不全と損傷が特徴の自己免疫疾患です。病原性自己抗体が、シナプス後膜上の特定のタンパク質を標的とすることにより、神経筋接合部におけるシナプス伝達が阻害されると考えられています。眼瞼下垂、複視、嚥下困難、咀嚼困難、発語困難などのさまざまな症状を有し、また、生命を脅かすような呼吸筋の筋力低下に至る可能性のある重度の筋力低下を引き起こすこともあります。
ジルビスクは、補体C5に結合しC5aおよびC5bへの開裂並びに、C5bおよびC6の結合を阻害する2つの作用によって神経筋接合部への補体が関与する損傷を阻害する次世代補体C5阻害剤です。1日1回の自己投与が可能で、全身型重症筋無力症(gMG)治療薬としては初の自己投与が可能な皮下注射剤として2023年11月22日に薬価収載されました。
今回の発売は、日本人を含む全身型重症筋無力症(gMG)患者さんを対象にジルビスクの有効性と安全性を検証した第III相国際共同試験(RAISE試験)に基づくものです。ジルビスクはプラセボ群に対して、主要評価項目であるMG-ADL総スコアの12週におけるベースラインからの変化量において統計学的有意に減少を示しました。
ユーシービージャパン株式会社の代表取締役社長の菊池加奈子氏は「昨年11月に発売したリスティーゴに続き、短期間に2剤目の重症筋無力症治療薬を患者さんにお届けできることを心より嬉しく思います。自己注射が可能なジルビスクは、治療の負担をより軽減し、患者さんのQOLの改善につながるものと期待しています。また、新たな患者サポートプログラムも同時に開始し、個々の患者さんに寄り添ったサービスの展開を行ってまいります」と述べています。