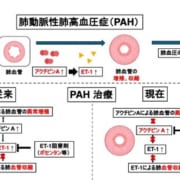
iPS細胞から作製した腎集合管オルガノイドを用いた多発性嚢胞腎モデルを活用し治療薬候補を発見
京都大学iPS細胞研究所(CiRA)は12月1日、iPS細胞から集合管を作製し、難病である多発性嚢胞腎の病態モデルを作製することに成功し、このモデルを活用して、治療薬候補の物質を見出したと発表しました。
多発性嚢胞腎は、腎臓に水が溜まった袋(嚢胞)が多数作られる進行性の難病です。腎臓の機能が徐々に低下していき、人工透析や腎移植を必要とする末期腎不全に至ります。中でも、常染色体顕性(優性)多発性嚢胞腎(ADPKD)では、主に集合管から嚢胞ができます。しかし、ヒト細胞を用いて、この症状を再現したモデルはありませんでした。これまでに、ヒトiPS細胞から作製した腎尿細管嚢胞モデルが作製されていましたが、ADPKDの治療薬候補は見つかっていませんでした。
今回、研究グループは、PKD1というADPKDの原因遺伝子をゲノム編集により変異体(PKD1-/-)にしたiPS細胞から集合管オルガノイドを作製し、多発性嚢胞腎(ADPKD)における集合管で嚢胞が形成されるモデルを構築しました。
まずはじめに、以前の研究で作製していた、健常人由来ヒトiPS細胞を、ゲノム編集によりPKD1-/-としたiPS細胞を用いて、集合管オルガノイドにおける嚢胞の形成を調べました。その結果、6週間以上拡大培養後に集合管へと誘導すると、嚢胞が自然に発生しました。この集合管オルガノイドにトルバプタンを作用させると嚢胞が縮小しました。

また、一度に96種の薬剤の効果を測定することができるスクリーニング系を確立し、AVPにより拡大した嚢胞のサイズを、強力なレチノイン酸受容体(RAR)作動薬であるTTNPBや、オールトランス型レチノイン酸(ATRA)での処理が抑制することがわかりました。

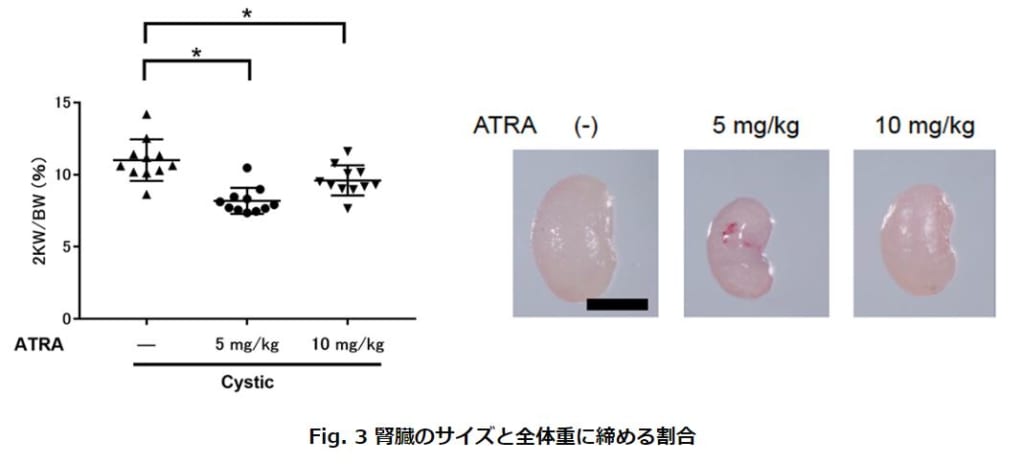
次に、多発性嚢胞腎(ADPKD)マウスモデルを用いて、他の疾患で使用されている治療薬である全トランス型レチノイン酸(ATRA)の効果を検証するため、生後3日目のマウスに、5または10mg/kgのATRAを腹腔内注射し、生後9日目に解析を行いました。ATRA投与による体重減少は観察されませんでしたが、体重に対する腎臓の重さの割合(2KW/BW)は、対照群と比較して、有意に減少しました。
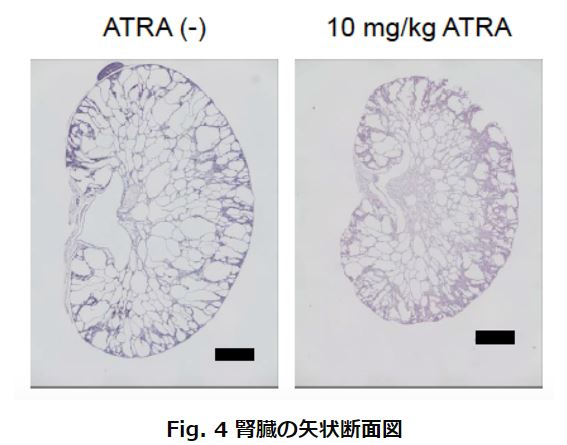
腎臓の断面を観察すると、10mg/kgのATRA処理群では、一部嚢胞の形成が抑制されていました。また、マウスの血液検査を行い、10mg/kgのATRA処理群は対照群と比べて腎機能の指標である血中尿素窒素値(BUN)の上昇が有意に抑制されていました。
以上の結果から、ヒトiPS細胞から作製した腎集合管オルガノイドを用いて作製した多発性嚢胞腎(ADPKD)マウスモデルを用いて、多発性嚢胞腎(ADPKD)の治療薬候補として、RAR作動薬を見出しました。実際に白血病の治療薬として使われているATRAが、マウスモデルにおいて嚢胞形成と腎機能増悪を抑制する効果があることが明らかになりました。
なお、今後、今回見出した薬剤候補を用いて、リジェネフロ社が近く治験を開始する見込みです。同研究の成果は、「Cell Reports」誌に、12月1日付で掲載されました。