フィンテプラ、ドラベ症候群に伴うてんかん発作治療薬として承認取得
ユーシービージャパン株式会社は9月26日、ドラベ症候群に伴うてんかん発作の治療薬の「フィンテプラ(R)内用液2.2mg/mL(一般名:フェンフルラミン塩酸塩)」に関して、「他の抗てんかん薬で十分な効果が認められないDravet症候群患者におけるてんかん発作に対する抗てんかん薬との併用療法」を効能・効果として、厚生労働省より製造販売承認を取得したことを発表しました。
ドラベ症候群は、1歳未満で発症するてんかん性脳症のひとつです。けいれんは発熱や入浴で誘発されやすく、けいれんを止めるために頻回の入院や救急医療が必要となります。また、重大な発達障害、運動障害、ならびにてんかんによる予期せぬ突然死(SUDEP)のリスクが高いといわれている指定難病です。
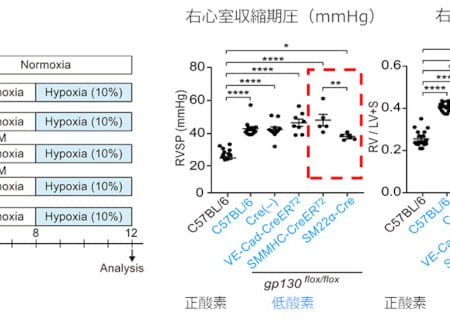
今回の承認は、小児および若年成人における既存の抗てんかん薬では発作が十分にコントロールできないドラベ症候群に対する国際共同無作為化二重盲検プラセボ対照第III相臨床試験を含む臨床開発プログラムの結果に基づくもの。日本人参加者を含む「試験3」において、けいれん発作回数のベースライン(プラセボ群)からの変化率は、フィンテプラ0.7mg/kg/日群で 64.8%(P<0.0001)の減少が認められ、主要評価項目を達成しました。また、今回の試験におけるフィンテプラの忍容性はおおむね良好で、既知の安全性プロファイルとも同様でした。なお、同剤は2021年8月に厚生労働省よりドラベ症候群における希少疾病用医薬品に指定されていました。
ユーシービージャパン代表取締役社長の菊池加奈子氏はプレスリリースにて、「既存の抗てんかん薬では治療が難しい希少てんかんであるドラベ症候群に対してフィンテプラが承認されたことを大変うれしく思います」と述べるとともに、「今回の承認は、てんかん領域をけん引する私たちの役割を希少疾患へ拡大するものです。フィンテプラが、乳幼児期に発症する難治性の高いてんかんを抱える⽇本の患者さんにとって新しい治療選択肢となり、患者さんやそのご家族が笑顔になることを心から願っております」と述べています。