DJ-1タンパク質によるcPGA分解機構がパーキンソン病発症抑制に寄与する可能性
東京科学大学は6月10日、遺伝性パーキンソン病の原因遺伝子DJ-1(PARK7)がコードするDJ-1タンパク質が、糖の代謝過程で生じる有害な副生成物cPGA(cyclic 3-phosphoglyceric anhydride)を分解する酵素として働く仕組みを、初めて明らかにしたと発表しました。さらに、遺伝性パーキンソン病患者さんが持つ変異によって、このDJ-1の酵素機能が損なわれることも明らかにしました。
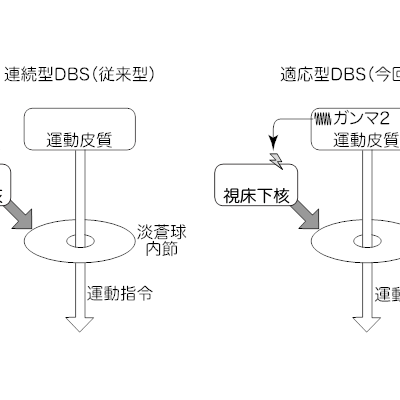
パーキンソン病(指定難病6)は、運動機能に障害を引き起こす進行性の神経変性疾患です。多くの症例は孤発性ですが、遺伝性のパーキンソン病も存在します。DJ-1は遺伝性パーキンソン病の原因遺伝子のひとつであり、その機能が失われると病気が発症することから、パーキンソン病の発症を抑える「パーキンソン病の抑制遺伝子」として知られています。これまでDJ-1タンパク質の細胞内での様々な役割が提唱されていましたが、その生理的に重要な機能は長らく不明でした。
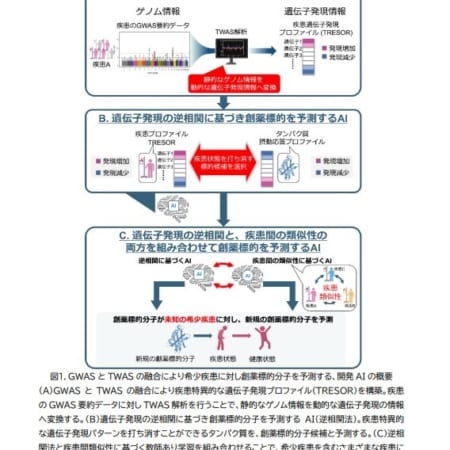
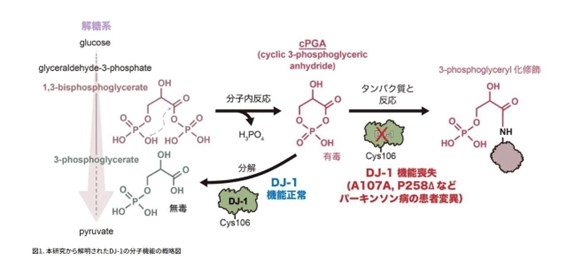
今回の研究の目的は、DJ-1タンパク質が有害な細胞内代謝物であるcPGA(cyclic 3-phosphoglyceric anhydride)を分解する酵素であることを証明し、その反応機構を分子レベルで解明することでした。cPGAは糖の代謝過程で生じる高反応性の副生成物であり、タンパク質などに非特異的な修飾を加えることで細胞障害を引き起こすことが知られています。
今回、研究チームは、DJ-1がcPGAを加水分解する酵素活性を持つことを明らかにしました。構造モデリングと生化学的解析により、DJ-1の求核性システインC106、オキシアニオンホールG74/G75、A107、P158、E18(cPGAとの相互作用部位)などのアミノ酸残基が、cPGAの分解反応を触媒する過程でどのように機能するかを示しました。さらに、パーキンソン病患者さんに見られるDJ-1の疾患関連変異であるA107PおよびP158Δが、DJ-1のcPGA分解酵素活性を完全に喪失させることを実証しました。
細胞内におけるDJ-1の生理的意義を検証するため、Phos-tagゲルを用いた独自の検出法や質量分析による解析が行われました。これらの解析から、DJ-1が欠損した細胞では、cPGA由来の修飾が異常に蓄積することが示されました。この結果は、細胞内においてcPGAの解毒にDJ-1が不可欠であることを実証するものです。また、従来DJ-1はメチルグリオキサールを解毒するグリオキサラーゼ活性を持つと考えられてきましたが、同研究では、DJ-1が欠損しても細胞内でメチルグリオキサールは蓄積せず、代わりにcPGAが蓄積することが示されました。このことは、細胞内におけるcPGAの解毒におけるDJ-1の重要性を示しています。
同研究では、DJ-1がcPGA分解酵素として機能し、その機能不全が強い毒性を持つ代謝物であるcPGAの蓄積を引き起こすことを分子レベルで解明。この発見は、若年性パーキンソン病の発症メカニズムの理解に新たな進展をもたらすものです。この研究成果により、パーキンソン病発症の新たな病態メカニズムを提唱するものであり、今後の創薬ターゲットの同定に貢献することが期待されます。また、同研究で確立された「DJ-1とcPGAの相互作用モデル」や「Phos-tagゲルを用いたcPGA修飾の可視化技術」は、他の反応性代謝物の研究や、神経変性疾患における代謝ストレスの理解にも応用可能であるとされています。
なお、同研究の成果は、「Journal of Cell Biology」に6月4日付で掲載されました。