筋萎縮性側索硬化症(ALS)患者さんの細胞外小胞におけるタンパク質組成の特徴を発見
慶應義塾大学とがん研究会がんプレシジョン医療研究センターの共同研究グループは7月22日、孤発性筋萎縮性側索硬化症(SALS)患者さんにおいて体液由来EVsのタンパク質組成が健常者と異なること、また、その変化が経時的なSALS病態進行においても同様に起こること、ロピニロール塩酸塩(ROPI)の投与によってこの変化が抑制されることを見出したと発表しました。
筋萎縮性側索硬化症(指定難病2)は、手・足・のどの筋肉や呼吸に必要な筋肉が徐々に痩せて力がなくなっていく疾患です。
細胞外小胞(EVs)は、ほとんどの細胞種から血液や脳脊髄液(CSF)などの体液中に分泌され、内部にタンパク質や核酸などを有していることから、細胞間の生体物質伝達に関わっているとされており、悪性腫瘍や孤発性ALS(SALS)などの神経変性疾患において疾患への寄与が推定されています。しかし、これまで孤発性ALS(SALS)における経時的かつ網羅的なEVタンパク質組成は明らかになっていませんでした。
今回、研究グループは、ロピニロール塩酸塩(ROPI)の第I/IIa相医師主導治験(ROPALS試験)のリバーストランスレーショナル研究(臨床現場において得られた知見をもとに、基礎研究を展開する手法のこと)として本研究を行い、経時的な患者由来体液を用いた網羅的なEVタンパク質組成を調べました。
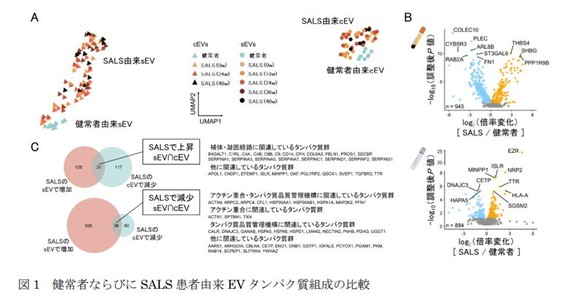
その結果、孤発性ALS(SALS)患者由来EVタンパク質組成は、健常者のものと比較して炎症に関与するタンパク質群が上昇し、タンパク質品質管理機構に関与するタンパク質群が減少していることがわかりました。
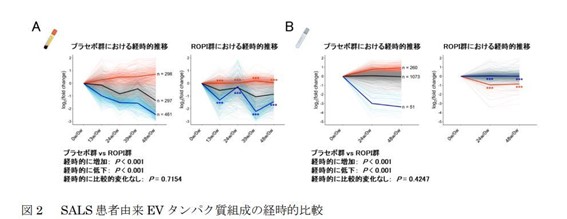
ROPALS試験では、13名のROPI群と7名のプラセボ群に分け、プラセボ群のデータを使用して、EVタンパク質組成の経時的変化を調べました。その結果、孤発性ALS(SALS)患者さんにおけるEVタンパク質組成は経時的に変化しましたが、ROPI投与によって当該変化が抑制されました。
さらに、ROPI投与によるタンパク質組成変化を明らかにするため、まずプラセボ群と ROPI群で比較を行いました。その後、コサイン類似度分析により、健常者-S孤発性ALS(SALS)患者比較、孤発性ALS(SALS)患者内の経時解析で同定されたタンパク質群との比較を行いました。その結果、ROPIによって、孤発性ALS(SALS)患者さんにおいて健常者と比して増加、ないし経時的に増加していたタンパク質群が抑制され、逆に孤発性ALS(SALS)患者さんにおいて健常者と比して減少、ないし経時的に減少していたタンパク質群が増加しました。
次に、iPastを用いた研究を行い、ROPIはD2R-CRYAB経路と呼ばれる神経炎症抑制に重要な経路を活性化することで、EVタンパク質組成変化を惹起している可能性が示唆されました。
ROPALS試験で収集された詳細な臨床データに基づき、EVs内のタンパク質を用いて筋萎縮性側索硬化症(ALS)の臨床指標となるバイオマーカーを探索した結果、予後予測ならびに診断において有用と推定されるタンパク質群をそれぞれ同定しました。
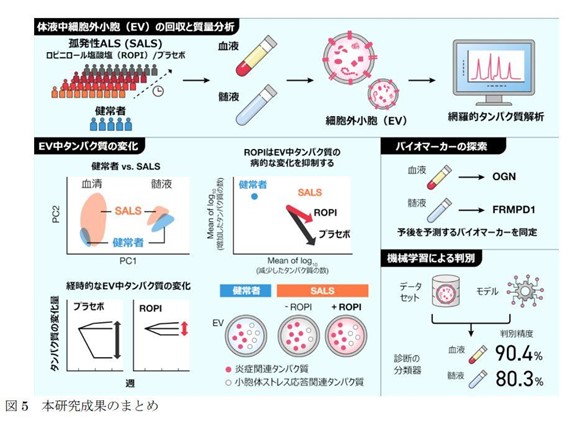
以上の研究成果より、EVsに内包されているタンパク質群が孤発性ALS(SALS)発症ならびに病態進行に寄与している可能性を示唆しており、ROPIによってそれら病的変化が抑制されることがわかりました。今後、EVsを用いた筋萎縮性側索硬化症(ALS)治療や、神経炎症抑制ないしプロテオスタシスの向上が筋萎縮性側索硬化症(ALS)治療戦略として有用である可能性が広がりました。
なお、同研究の成果は、「Inflammation and Regeneration」誌に7月12日付で掲載されました。
────────────────────────────────────────────────
【レアズからのお知らせ】
ALSの患者さん 臨床研究(インタビューまたはアンケート調査)のご案内
────────────────────────────────────────────────