バイスペシフィック抗体バビースモが新生血管を伴う網膜色素線条を対象としたで視力改善を示す
中外製薬株式会社は4月15日、バビースモ(一般名:ファリシマブ)について、新生血管を伴う網膜色素線条を対象とした国内第III相臨床試験(NIHONBASHI試験)において、主要評価項目を達成し、12週時点において統計学的に有意かつ臨床的に意義のある視力改善を確認したと発表しました。
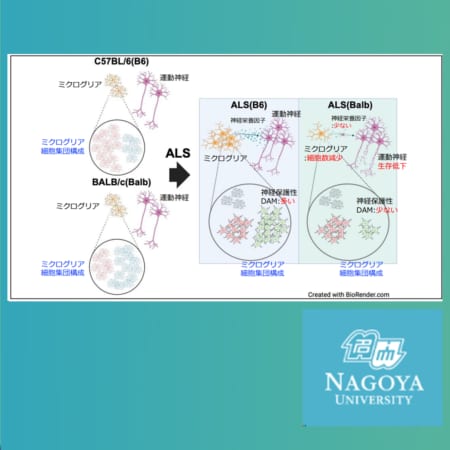
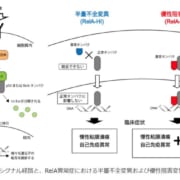
網膜色素線条は、網膜の一部が断裂し、眼底に特徴的な線状の色調変化(色素線条)がみられる疾患。眼底の中央の黄斑部に脈絡膜新生血管がおよぶと視力低下やゆがみなどの症状が現れます。新生血管を伴う場合は、従来の手術やレーザーなどの治療では十分な効果を得ることが難しく、予後不良であるため、新たな治療法の開発が望まれています。また、同疾患の国内における患者数は不明であり、網膜色素線条を約半数で合併すると知られる指定難病のひとつ「弾性線維性仮性黄色腫(指定難病166)」の患者数は約300名とされています。
バビースモは、眼科領域における初のバイスペシフィック抗体(二重特異性抗体)です。同剤は、視力を脅かす多くの網膜疾患に関連する2つの疾患経路、アンジオポエチン-2(Ang-2)と血管内皮増殖因子-A(VEGF-A)を標的として阻害し、血管を安定させるよう設計されています。
今回の試験において、バビースモの忍容性はおおむね良好であり、新たな安全性上の懸念は示されませんでした。
中外製薬の代表取締役社長CEOの奥田修氏はプレスリリースにて、「網膜色素線条は、国内において承認された治療薬がない希少疾病です。本疾患を対象にした試験において、バビースモが日本人で初めて良好な視力改善を示したことを大変嬉しく思います。一日でも早く患者さんにお届けできるよう、日本での承認申請に向けて尽力してまいります」と述べています。
なお、今回の試験の成績は、実施国である日本の規制当局に提出を予定しており、今後の医学系学会で発表される予定です。