既存治療で効果不十分な乾癬性関節炎・強直性脊椎炎およびX線基準を満たさない体軸性脊椎関節炎に対するビンゼレックスの適応追加の承認を取得
ユーシービージャパン株式会社は12月22日、ヒト化抗ヒトIL-17A/IL-17Fモノクローナル抗体製剤「ビンゼレックス皮下注160mgシリンジ、同皮下注オートインジェクター」(一般名:ビメキズマブ(遺伝子組換え)以下、ビンゼレックス)について、既存治療で効果不十分な乾癬性関節炎(PsA)、強直性脊椎炎(AS)およびX線基準を満たさない体軸性脊椎関節炎(nr-axSpA)への適応拡大について厚生労働省より承認を取得したと発表しました。
乾癬性関節炎(PsA)は、乾癬という皮膚の病気に関節の痛みや腫れを伴う関節炎を合併する全身性炎症性疾患です。国内では乾癬患者さんの約15%が乾癬性関節炎(PsA)を有しているといわれています。
強直性脊椎炎(AS)およびX線基準を満たさない体軸性脊椎関節炎(nr-axSpA)は、体軸性脊椎関節炎に分類される慢性の自己免疫による炎症性疾患です。仙腸関節の構造的障害を示す確定的なX線所見が認められる場合は強直性脊椎炎(AS)、認められない場合は体軸性脊椎関節炎(axSpA)となります。多くの場合、腰背部痛を認め、安静では軽快せず、運動で改善するという特徴があります。
ビンゼレックスは、炎症性疾患の発症に重要な役割を果たしている炎症性サイトカインであるIL-17AとIL-17Fをともに選択的かつ直接的に阻害する唯一のヒト化モノクローナルIgG1抗体です。IL-17Aのみならず、IL-17Fも選択的に阻害することで、IL-17Aのみの阻害よりさらに大きな炎症抑制が期待されます。
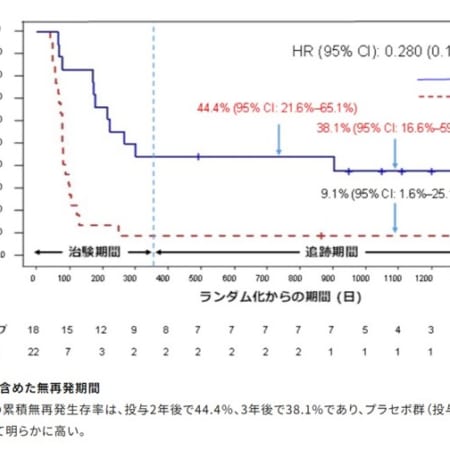
今回の乾癬性関節炎(PsA)に対する承認申請は、第Ⅲ相BEOPTIMAL試験およびBE COMPLETE試験に、強直性脊椎炎(AS)とX線基準を満たさない体軸性脊椎関節炎(nr-axSpA)に対する承認申請は、BE MOBILE1試験およびBEMOBILE2試験のデータに基づいたものです。これら4つの試験において、ビンゼレックスはプラセボに対して有効性を示したとともに、すべての試験において、安全性のプロファイルは、同剤の過去の試験データと一致しており、新たな安全性シグナルは認められませんでした。
代表取締役社長の菊池加奈子氏は「ビンゼレックスは、昨年、尋常性乾癬、膿疱性乾癬、乾癬性紅皮症に対して承認され、販売を開始しました。今回の適応拡大によって、このIL-17AとIL-17Fをともに選択的かつ直接的に阻害する治療薬が、さらに多くの患者さんの治療選択肢となることを期待し、患者さんとそのご家族の笑顔につながるよう貢献してまいります」と述べています。
なお、第Ⅲ相BE OPTIMAL試験およびBE COMPLETE試験のデータは「The Lancet」に掲載されました。また、BE MOBILE1試験およびBE MOBILE2試験のデータは「Annals of the Rheumatic Diseases」に掲載されました。