SPECIAL
【治験広告】甲状腺眼症にお困りの方へ 新たなお薬のご紹介です

本ページは、argenx BV社からの委託による治験広告となります。
また、治験を実施する治験実施医療機関の審査・承認を受けたものを掲載しております。
はじめに
本治験は甲状腺眼症の患者さんを対象とした新しいお薬の治験です。
治験参加にはメリット、デメリットがありますので主治医の先生やご家族とご相談の上でご参加ください。
甲状腺眼症とは
甲状腺眼症とは、甲状腺に関係した抗体が眼球の周りにある脂肪や目を動かす筋肉の中に存在し、それが標的となって炎症が起こる疾患です。 甲状腺機能亢進症(バセドウ病)でも低下症(橋本病)でも、また甲状腺機能が正常であっても甲状腺眼症は起こります。 甲状腺機能の異常による全身の症状が目の症状よりも先に現れるかどうかは、患者さんによってさまざまです。
治験とは
臨床試験とは、薬に関する特定の課題に対する答えを見つけ出すための医学的な研究です。どの新薬も、医師が患者さんに処方するためには、その前に臨床試験を行わなければなりません。臨床試験を行わずに新薬は開発できません。
新薬を開発するためには、まず動物を用いて、候補となる薬の効き目(有効性)や安全であるか否か(安全性)について確認する必要があります。その後、多数の患者さんにご協力いただき、その薬を使用して、ヒトでの有効性や安全性を調べます。薬などを患者さんに使用して有効性や安全性を確認するために行う試験を総称して「臨床試験」といいます。臨床試験のうち、薬が厚生労働省に承認される前に実施される試験を「治験」と呼んでおり、「治験」で使用される薬を「治験薬」と呼んでいます。
治験で収集されたデータは、患者さんと同じ病気にかかっている他の患者さんの治療薬を開発するために役立ちます。現在販売されている薬の大半に関しても、多くの人々の協力を得て治験が行われています。
治験の参加条件
- ・18歳以上の方
- ・症状が重いほうの眼について、自己免疫性甲状腺疾患(バセドウ病または橋本甲状腺炎)に伴う
中等度から重度の活動性の甲状腺眼症と臨床的に診断された治験担当医師が判断した方 - ・12か月以内に活動性の甲状腺眼症の症状を最初に発症した方
- ・基礎疾患がコントロールされており甲状腺機能正常であるか、甲状腺機能低下症または甲状腺機能亢進症が軽度である方
この他にも細かな条件がありますので、詳細はお問い合わせ時にご確認ください。
また、ご自身で判断ができない参加条件がある場合もお気軽にお問い合わせください。
※本試験ではすでに甲状腺眼症と診断された方向けではありますが、現在症状でお悩みの方も受診し、診断を受けることでご参加いただけることがあります。
レアズ内に甲状腺眼症についてまとめた記事がございます。ぜひご参考にご一読ください。
→「甲状腺眼症」(こうじょうせんがんしょう)についてコチラ
※下記に甲状腺疾患にて代表とされる諸症状を列挙いたしますが、ご心配事がおありでしたらかかりつけ医などへ相談をお勧めいたします。
代表的な諸症状:疲れやすくなる、落ち着きが無い、不眠、便の状態が変わる(軟便や便秘)、首が太くなる、目が出て見えたり瞼が腫れる、など。
お問い合わせはコチラ
治験の目的
甲状腺眼症の患者さんを対象として、治験薬の安全性と有効性(効き目)を評価することを目的としています。この試験では、治験薬がどのように吸収され体から排出されるかを調べます。また、患者さんの免疫系が治験薬に対してどのように反応するかについても調べます。
患者さんの症状が改善したり、またはこの試験への参加による利益をうけることはないかもしれません。この治験から得られる情報が将来的に甲状腺眼症の他の患者さんの役に立つかもしれません。
これらの段階を経て、得られたデータが厚生労働省に提出され、審査を経て承認されると、新しい薬として広く使用できるようになります。
治験は、新しい薬の開発に不可欠なプロセスであり、患者さんの健康と安全を守るために非常に重要な役割を果たしています。
治験薬について
今回の治験薬は、FcRn(胎児性Fc受容体)と呼ばれる特定のたんぱく質に結合しやすいようにしたヒトの抗体の一部使用した生物学的製剤の注射薬です。
哺乳類の細胞の中で作られたたんぱく質であることから、「生物学的」製剤と呼ばれます。
抗体とは、感染症と闘って、感染症の発症を防ぐたんぱく質です。FcRnには抗体の量を維持する役割があります。
この治験薬は、ヒトの身体に生まれつき存在している抗体と類似しています。
治験薬は、重症筋無力症(筋力の低下を引き起こす稀な疾患)の成人患者さんの治療薬として既に承認されており、他の自己免疫性疾患(自分の免疫系が自分の体の一部を攻撃する疾患の総称)の治療薬としても研究されています。
甲状腺眼症の治療薬としては承認を受けていないため、この治験にて効果と安全性を調べています。
有害な抗体を減らすことで甲状腺眼症の改善に役立つ可能性があるのではないかと、この治験薬が開発されました。
お問い合わせはコチラ
治験の方法
週に1回、24週間、治験薬の皮下注射を受けていただきます。
この治験の継続期間は、患者さんが治験薬にどのように反応するかによって異なり、1年から2年の間です。
この治験には以下の期間が含まれます。
実際に治験に参加できるか検査等で調べます。
実施医療機関にもよりますが、1~2回のご通院になります。
どの治療を誰が受けているかを、患者さんも治験のスタッフも分からない期間のことを意味します。
この期間に、患者さんは治験薬かプラセボ(見た目は本物の薬とそっくりですが、有効成分を含まない偽薬)の投与を受けます。
初回の投与と1・4・6・12・18・24週目にご通院いただきます。(計7回)
ただし、治験薬投与のために毎週来院して投与を頂く場合は、通院頻度が増える場合があります。
参加頂く病院によっては自宅での投与も認められます。
その後も体調に変化がないかなどを確認いたします。
初回の投与から30・40・52・64・76週目にご通院いただきます。(計5回)
この期間に、患者さんは治験薬の投与を受けます。
第二の投与開始時と1・6・12・24週目にご通院いただきます。(計5回)
上記以外にも患者さんの治験薬への反応に応じて、最大22回、治験実施医療機関に来院していただきます。
この回数は、患者さんの状態や意向によって変わります。
一部の来院時には、検査をいくつか受けていただきます。
お問い合わせはコチラ
実施医療機関所在地(2025年11月4日更新)
・宮城県仙台市
・茨城県水戸市
・大阪府大阪市
・長崎県長崎市
※上記の医療機関は、総合病院や大学病院等です。
※実際の治験実施医療機関名は参加の可能性がある患者さんにお伝えします。
※IRB承認状況と実際の募集状況により記載は変更されます。
お問い合わせはコチラ
治験に参加した場合の費用負担
原則として治験に参加している間の治験に関わる検査費用や薬剤費等は、治験を実施している製薬会社が負担します。さらに、治験に参加される方の交通費等の負担を軽減するために一定額の「負担軽減費」の支払いがあります。詳しくはレアズコンタクトセンターにお問い合わせください。
一方、治験に関係しない費用(診察料や他の病気に対する医療費など)についてはご自身のご負担となります。
お問い合わせ
お申込みは24時間応募可能な「アンケート」からのお申込みが便利です。
専門スタッフがアンケート回答を確認後、ご希望の方法(メール・電話)にてご連絡を差し上げます。
■お電話で問い合わせる

*スマートフォンのみ、タップで架電します
電話番号:0120-330-800(平日10:00-18:00)
※お電話口で「甲状腺眼症の治験について」とお伝えください
■お問い合わせフォームから問い合わせる

・お問い合わせ項目:「サイトへのお問い合わせ」を選択してください。
・お問い合わせ詳細:「甲状腺眼症の治験について」とご入力ください。また、お問い合わせ内容をご入力ください。
※治験の参加条件に該当しているかどうか確認したい場合は、お電話にてお問い合わせください。
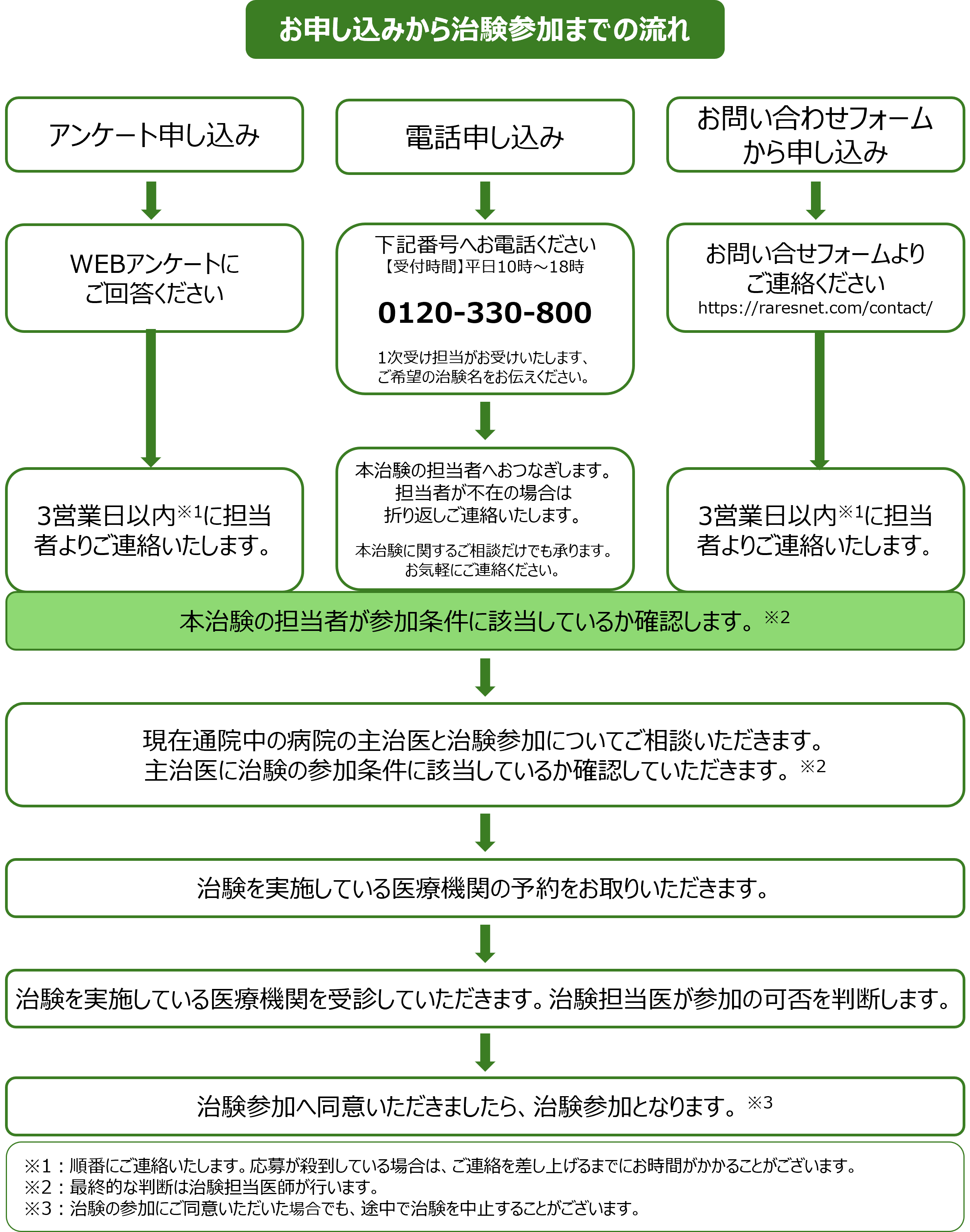
お申し込みから治験参加までの流れ
主治医向けページ
主治医(医療従事者)の方はこちらから本治験の詳細とご紹介の流れをご確認いただけます。

個人情報の取扱いについて
あなたの個人情報は保護され、あなたが許可する場合または法律で必要とされる場合を除き、「レアズ」の当該治験の担当スタッフ、あなたの担当医および治験実施施設のスタッフのみが共有します。
それ以外の人には、あなたの個人情報が開示されることはございません。
「レアズ」の個人情報の取扱いについてはコチラ
広告主体者:3Hメディソリューション株式会社/3Hメディソリューション株式会社は日本CRO協会賛助会員です。

