リツキサン、難治性尋常性天疱瘡および落葉状天疱瘡に対する承認を取得
全薬工業株式会社と中外製薬株式会社は2021年12月24日、両社で共同販売を行っている抗CD20モノクローナル抗体「リツキサン(R)点滴静注100 mg、同500 mg」(一般名:リツキシマブ(遺伝子組換え))ついて、「難治性の尋常性天疱瘡及び落葉状天疱瘡」を効能または効果として、厚生労働省より製造販売承認を取得したと発表しました。
天疱瘡は、皮膚・粘膜に病変が見られる自己免疫性水疱性疾患。性別比では、男:女=1:1.5と女性に多く、50歳代~60歳代に多い疾患です。日本における天疱瘡患者さんは約3,000例といわれており、リツキサンの対象となる「難治性天疱瘡」の患者さんは500例ほどと推測されます。なお、天疱瘡は厚生労働省によって難病指定を受けておいます(指定難病35)。
今回の承認は、ステロイド治療で効果不十分な天疱瘡患者さんを対象に、慶應義塾大学病院を拠点として日本国内で行われた医師主導の国内第II相臨床試験である「KCTR-D006試験ならびにスイス・ロシュ社主導の海外第III相臨床試験である「PEMPHIX試験」の結果に基づいています。
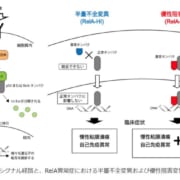
リツキサンは、B細胞上に発現するタンパク質のCD20抗原に特異的に結合する抗CD20モノクローナル抗体。標的となるB細胞をヒトの体内に備わった免疫系を用いて攻撃し、細胞を傷害します。